Instrucciones
Usted tiene las siguientes opciones en este simulador para moléculas pequeñas tanto inorgánicas como orgánicas.
- En la parte superior, aparecen los botones 2D y 3D para que pueda observar el modelo en dos o tres dimensiones.
- A continuación se presenta el modelo en dos o tres dimensiones.
- "Search" puede ser utilizado para buscar alguna molécula, escribiendo el nombre en inglés, por ejemplo al escribir, sulphuric acid (ácido sulfúrico).
- Color de fondo, sirve seleccionar el color del fondo del modelo en tres dimensiones.
- Acercar +, acerca el modelo.
- Acercar -, aleja el modelo.
- Girar X, Y, Z, para girar el modelo en tres dimensiones en los ejes x, y, z.
- Alambres, varillas y pelotas y varillas, para cambiar el modelo en tres dimensiones en esas representaciones.
- Energía, aparce en la parte superior la energía de la molécula en kJ/mol o kcal/mol.
- Minmizar por MMFF94, normalmente las estructuras iniciales que se crean en los simuladores poseen energías mucho mayores a las que tendría un objeto real, por esta razón, se utilizan algoritmos para calcular las posiciones y fuerzas originales, con el objetivo de minimizarlas y que sean más realistas.
- Arrastrar Minimizar, usted puede arrastrar un átomo, soltarlo y entonces el sistema hace un cálculo de minimización de energía.
- Simetría, muestra los planos de simetría en la molécula.
- Editar, puede editar la molécula agragando o quitando átomos y enlaces.
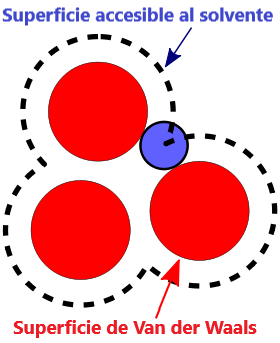
- Superficie VDW, la superficie de van der Waals de una molécula es una representación abstracta o modelo de esa molécula, que ilustra dónde, en términos muy generales, podría haber una superficie para la molécula en función de los cortes duros de los radios de van der Waals para átomos individuales, y representa una superficie a través de la cual la molécula podría concebirse interactuando con otras moléculas.
- PEM es el mapa de potencial electrostático.
- Carga parcial calcula la carga parcial de cada átomo.
- Tetraedros, para el caso que exista alguna átomo tetraédrico.
- Dipolos enlaces, para ver el los dipolos de todos los enlaces.
- Dipolo molecular, para ver el momento dipolar resultante de toda la molécula.
- Hibridación sp, sp2 y sp3, para ver la hibridacion del átomo de carbono.
- Anillo aromático, muestra los anillos aromáticos.
- Heteroátomo, muestra los heteroátomos en heterociclos.
- C quiral (nomenclatura R/S) y E/Z para isomería geométrica en alquenos, los descriptores R/S permiten indicar en un compuesto orgánico la configuración (la disposición espacial de los sustituyentes) de un carbono o centro quiral, estereocentro o centro estereogénico, que es el caso de un átomo de carbono con cuatro sustituyentes diferentes. Se añade R o S entre paréntesis como prefijo delante del nombre de la molécula orgánica. En caso de ser más de uno el centro estereogénico, separados por coma se indica el descriptor R o S de cada uno, precedido del número o localizador que identifica su posición.
- Invertir R/S, para cambiar la quiralidad.
- Nomenclatura E/Z en Alquenos, el sistema tradicional para nombrar los isómeros geométricos de un alqueno, en el que los mismos grupos están dispuestos de manera diferente, es nombrarlos como cis o trans. Sin embargo, es fácil encontrar ejemplos donde el sistema cis-trans no se aplica fácilmente.
- N electrones, O electrones y S electrones, para ver los electrones libres del nitrógeno, oxígeno y azufre.
- C primario, C secundario, C terciario, C cuaternario, identifica la clasificación de los átomos de carbono.
- Dadores y aceptores de puentes de hidrógeno, señala los átomos que pueden dar o aceptar puentes de hidrógeno
- Botón 2D, cuando escoge el botón 2D, la aplicación tiene su propio menú y quedan inhabilitados todos los botones 3D.<
Laboratorio de IA: Tu Copiloto de Estudio
Aprende a usar la Inteligencia Artificial Científica
La IA no sirve solo para dar respuestas, sino para profundizar el pensamiento hipotético y matemático. Si eres estudiante del Profesorado de Física-Matemática, aquí tienes 4 "Prompts" avanzados para desafiar tu comprensión analítica de los Coloides:
1. Cielos Azules y Nubes Blancas
El Efecto Tyndall explicado.
2. Einstein y los Átomos
El Movimiento Browniano.
3. La Física de un Filtro Médico
Presión y Diálisis.
4. Experimento Divertido con Láser
Prácticas para enseñar Óptica de Dispersiones.
Simulador: El Efecto Tyndall
Comprende de forma visual y microscópica la diferencia óptica entre una solución, un coloide y una suspensión a través de esta experiencia interactiva.
Nota: Enciende el láser virtual y mueve la altura para observar cómo reacciona el haz de luz ante diferentes tamaños de partículas.
Laboratorio: Filtración y Membranas
Experimenta con diferentes tipos de membranas y observa qué partículas (soluciones, coloides o suspensiones) logran atravesarlas.
Nota: Este simulador ilustra de forma interactiva el principio de la diálisis y el funcionamiento de los capilares sanguíneos.
Coloides
Los Sistemas de Dispersión en Medicina
En el cuerpo humano y en la práctica clínica, rara vez trabajamos con sustancias puras. La gran mayoría de los fluidos biológicos y de las preparaciones farmacológicas son sistemas de dispersión. Estos sistemas están formados por una sustancia que se dispersa (fase dispersa o soluto) dentro de otra sustancia en la que se distribuye (medio dispersante o fase continua).
La diferencia fundamental entre los distintos tipos de mezclas radica en el tamaño de las partículas de la fase dispersa. Este tamaño determina si la mezcla se comportará como una solución, un coloide o una suspensión, lo cual es vital para entender cómo interactuará con las membranas celulares del paciente.
1. Soluciones Verdaderas
Tamaño de partícula: Menor a 1 nm (< 10-9 m).
Son mezclas perfectamente homogéneas. Las partículas (iones o moléculas pequeñas) están disueltas a nivel individual. No se asientan con la gravedad, no pueden separarse por filtros ni por membranas biológicas, y son totalmente transparentes (no dispersan la luz).
Ejemplo Clínico: Suero fisiológico (NaCl al 0.9%) o soluciones glucosadas. La glucosa y los iones de sodio difunden con el agua a través de los tejidos.
2. Coloides
Tamaño de partícula: Entre 1 nm y 100 nm.
Representan un estado límite. Las partículas son macromoléculas (proteínas) o agregados moleculares. Pasan a través de filtros ordinarios, pero son retenidas por membranas biológicas semipermeables (como los endotelios capilares). Además, dispersan la luz (Efecto Tyndall).
Ejemplo Clínico: El plasma sanguíneo (donde la proteína coloidal 'albúmina' retiene el agua en las venas), gelatinas o el interior celular.
3. Suspensiones
Tamaño de partícula: Mayor a 100 nm.
Son mezclas heterogéneas. Las partículas son tan grandes que sedimentan al reposar por la fuerza de gravedad y pueden separarse mediante filtros ordinarios de laboratorio.
Ejemplo Clínico: La sangre entera (células que flotan temporalmente en el plasma), jarabes antibióticos pediátricos (requieren la indicación "Agítese antes de usar").
Cuadro Comparativo de Dispersiones
| Característica | Soluciones Verdaderas | Coloides | Suspensiones |
|---|---|---|---|
| 1. Tamaño de partícula | Menor a 1 nm | Entre 1 nm y 1000 nm | Mayor a 1000 nm |
| 2. Fases presentes | Una sola fase | Dos fases (dispersa y dispersante) | Dos fases |
| 3. Homogeneidad | Totalmente homogénea | En el límite (heterogénea al microscopio) | Heterogénea |
| 4. Separación al reposar | No se separa / No sedimenta | No se separa / No sedimenta | Se separa y sedimenta por gravedad |
| 5. Transparencia | Transparente (no dispersa la luz) | Traslúcida (presenta Efecto Tyndall) | No transparente / Opaca |
Explicación de las Características
- 1 Tamaño de partícula
- Es el criterio principal para clasificar estas mezclas. Las soluciones verdaderas contienen partículas tan diminutas (iones o moléculas simples) que no pueden ser vistas ni filtradas. Los coloides tienen partículas más grandes (como las proteínas plasmáticas). En las suspensiones, las partículas superan los 1000 nm, siendo tan grandes que a veces son visibles a simple vista o con microscopios convencionales.
- 2 Fases presentes
- Una solución es un sistema monofásico; el soluto y el solvente se integran tan íntimamente que forman una sola fase indistinguible. Los coloides y las suspensiones son sistemas difásicos (dos fases): están compuestos por una "fase dispersa" (las partículas) que flota dentro de un "medio dispersante" (el fluido que las rodea).
- 3 Homogeneidad
- Las soluciones son mezclas completamente homogéneas en cualquier proporción. Las suspensiones son claramente heterogéneas. Los coloides se encuentran en un estado límite: parecen homogéneos a simple vista (como la leche o la gelatina), pero al observarlos a nivel ultramicroscópico revelan su naturaleza heterogénea.
- 4 Separación al reposar
- Las partículas en las soluciones y los coloides están en constante movimiento térmico (movimiento Browniano) que vence a la fuerza de gravedad, por lo que nunca se asientan en el fondo. En contraste, las partículas de una suspensión son tan pesadas que terminan sedimentándose con el tiempo por efecto de la gravedad.
- 5 Transparencia
- Las soluciones permiten el paso libre de la luz, mostrándose transparentes. Los coloides son típicamente traslúcidos y tienen la propiedad única de dispersar un haz de luz que los atraviesa (fenómeno conocido como Efecto Tyndall). Las suspensiones suelen ser opacas o muy turbias y bloquean el paso de la luz.
¿Por qué es importante en medicina?
Comprender estas diferencias permite al personal médico administrar medicamentos adecuadamente. Por ejemplo, nunca se debe inyectar una suspensión por vía intravenosa, ya que las partículas grandes podrían causar una embolia (taponamiento de un vaso capilar). Por otro lado, los coloides se usan en urgencias para expandir el volumen de sangre porque sus grandes moléculas no pueden escapar de los vasos sanguíneos hacia los tejidos, a diferencia de las soluciones verdaderas (cristaloides) que sí difunden rápidamente.
Anatomía de un Coloide
Para entender los coloides, es fundamental conocer sus dos componentes principales, que son el equivalente al "soluto" y "solvente" de las soluciones verdaderas:
- Fase Dispersa (o sustancia dispersada): Es la sustancia que se encuentra en menor proporción, distribuida en forma de partículas (tamaño 1 a 1000 nm). En la leche, por ejemplo, la fase dispersa son las gotitas de grasa y las proteínas.
- Medio Dispersante (o fase de dispersión): Es la sustancia continua en la cual las partículas coloidales están distribuidas o "flotando". En la leche, el medio dispersante es el agua.
Clasificación según su estado físico
Dependiendo del estado físico de la fase dispersa y del medio dispersante, los coloides reciben diferentes nombres. Memorizar los más comunes (como emulsiones o geles) es clave en el área biomédica y farmacéutica:
| Clase de Coloide | Medio Dispersante | Sustancia Dispersa | Ejemplos Comunes y Clínicos |
|---|---|---|---|
| Soles, geles | Líquido | Sólido | Gelatina, plasma celular, geles para ecografía |
| Emulsiones | Líquido | Líquido | Leche, mayonesa, cremas dermatológicas, propofol (anestésico IV) |
| Espumas | Líquido | Gas | Espuma de jabón, crema batida, espumas espermicidas |
| Aerosoles líquidos | Gas | Líquido | Neblina, nubes, sprays inhaladores (ej. Salbutamol) |
| Aerosoles sólidos | Gas | Sólido | Humo, polvo suspendido en el aire |
| Espumas sólidas | Sólido | Gas | Caucho, esponjas, piedra pómez |
| Emulsiones sólidas | Sólido | Líquido | Queso, mantequilla |
| Sol sólido | Sólido | Sólido | Algunas aleaciones, vidrio rubí, porcelana |
¿Qué son las Emulsiones Coloidales?
Una emulsión es un tipo específico de coloide donde tanto la fase dispersa como el medio dispersante son líquidos inmiscibles (que normalmente no se mezclan, como el agua y el aceite). Para que una emulsión coloidal sea estable y las gotas microscópicas no se vuelvan a unir por repulsión, se requiere de un tercer componente crucial llamado agente emulsionante.
El Rol del Agente Emulsionante
Estas moléculas tienen una parte hidrofílica (afín al agua) y otra lipofílica (afín a las grasas). Se colocan en la frontera protectora entre la gota de líquido disperso y el medio, estabilizando el sistema. En el cuerpo humano, las sales biliares actúan como emulsionantes naturales esenciales para poder digerir las grasas en el intestino.
Importancia Clínica
Muchos medicamentos intravenosos son insolubles en agua. El Propofol, un potente anestésico general, se formula como una emulsión coloidal lechosa (gotitas de aceite de soya en agua, usando lecitina de huevo como emulsionante) para poder ser inyectado en el torrente sanguíneo de forma segura.
Diferencia entre Sol y Gel
Es común encontrar o confundir estos dos términos, ya que muchas sustancias pueden alternar entre ambos estados dependiendo de factores como la temperatura o la concentración:
Estado Sol (Líquido)
Es una dispersión coloidal donde la fase dispersa es un sólido y el medio dispersante es un líquido. A simple vista, tiene el comportamiento y la fluidez de un líquido.
Ejemplo: Gelatina caliente (cuando está líquida), el citoplasma celular en estado fluido, pintura fresca.
Estado Gel (Semisólido)
Es un sistema donde las partículas sólidas se entrelazan formando una red tridimensional que atrapa al líquido. Aquí la fase dispersa es el líquido y el medio continuo actúa como un sólido. Pierde su capacidad de fluir fácilmente.
Ejemplo: Gelatina fría (cuajada), un coágulo de sangre, geles para ecografía.
¿Existen las "Suspensiones Coloidales"?
Es muy común escuchar el término suspensión coloidal en la práctica médica y farmacológica. Aunque en la fisicoquímica pura se prefiere llamarlas dispersiones coloidales (o específicamente un Sol, al ser un sólido en un líquido) para evitar confusiones con las suspensiones "ordinarias" o groseras, el término es válido y de uso extendido.
La Diferencia Clave
Cuando un texto médico habla de una suspensión coloidal, se refiere a un líquido que contiene partículas sólidas microscópicas (de tamaño entre 1 y 1000 nm) que no se asientan en el fondo con el tiempo. Se mantienen flotando indefinidamente gracias a los constantes choques del líquido circundante (Movimiento Browniano) y a la repulsión de cargas eléctricas en su superficie. Si estas partículas pierden su carga eléctrica, se unen, superan los 1000 nm y decantan por gravedad, pasando a ser una suspensión común.
Afinidad por el Medio Dispersante
La Realidad Clínica: Sistemas Mixtos de Dispersión
En teoría, dividimos las mezclas en tres cajas perfectas (soluciones, coloides y suspensiones). Sin embargo, en el cuerpo humano, los fluidos biológicos reales suelen tener características múltiples al mismo tiempo.
El mejor ejemplo es la Sangre Humana:
- Es una Suspensión porque contiene eritrocitos, leucocitos y plaquetas que son lo suficientemente grandes como para sedimentar por gravedad (de ahí que podamos medir clínicamente la velocidad de sedimentación globular - VSG).
- Es un Coloide si observamos solo el plasma, ya que contiene grandes proteínas globulares (como la albúmina) que no se asientan ni atraviesan las paredes de los capilares sanguíneos sanos.
- Es una Solución Verdadera porque en esa misma agua del plasma hay disueltos electrolitos (sodio, potasio) y glucosa que son menores a 1 nm.
Comportamiento Físico y Métodos de Separación
A modo de resumen, la siguiente tabla detalla cómo se comportan las mezclas frente a la gravedad y frente a diferentes barreras físicas. Este cuadro es fundamental para la clínica y la resolución de guías de estudio:
| Comparación | Tipo de mezcla | Tipo de partícula | Asentamiento | Separación |
|---|---|---|---|---|
| Solución | Homogénea | Pequeñas (iones, átomos o moléculas simples) | No se asientan | No se pueden separar con filtros ni con membranas |
| Coloide | Límite (Aparenta homogénea, es heterogénea) | Grandes (macromoléculas o grupos de moléculas) | No se asientan | Se pueden separar con membranas (Diálisis), pero no con filtros |
| Suspensión | Heterogénea | Muy grandes (a veces visibles a simple vista) | Se asientan rápidamente (sedimentan) | Se separan fácilmente con filtros ordinarios |

Los coloides poseen propiedades ópticas y cinéticas muy particulares que los diferencian de las soluciones verdaderas y de las suspensiones ordinarias.
Efecto Tyndall
Es el fenómeno de dispersión de la luz causado por las partículas coloidales. Cuando un haz de luz (como un láser o un faro) atraviesa un coloide, su trayectoria se hace visible porque las partículas son lo suficientemente grandes para desviar los fotones.
En una solución verdadera, las partículas (iones o moléculas) son tan diminutas que la luz pasa sin desviarse, por lo que la trayectoria del rayo de luz es invisible.

Movimiento Browniano
Es el movimiento caótico, rápido y en forma de zigzag que experimentan las partículas coloidales. Se produce por los constantes choques y bombardeos desiguales de las moléculas del medio dispersante contra las partículas dispersas.
Este movimiento cinético es de vital importancia porque vence a la fuerza de gravedad; es la razón principal por la que las partículas de un coloide no se asientan ni sedimentan en el fondo con el paso del tiempo.

Aunque teóricamente clasificamos las mezclas de forma estricta por el tamaño de sus partículas (menores de 1 nm para soluciones, hasta 1000 nm para coloides y mayores a eso para suspensiones), en la práctica del laboratorio y en la naturaleza las fronteras pueden ser difusas. A continuación, exploramos casos donde las sustancias presentan un comportamiento intermedio o dual:
1. El Almidón

El almidón en agua fría no se disuelve y tiende a comportarse como una suspensión (se asienta en el fondo). Sin embargo, al calentar el agua, los gránulos se hinchan y se rompen, liberando macromoléculas (amilosa y amilopectina) que forman una dispersión coloidal viscosa o un gel que ya no sedimenta.
2. Leche de Magnesia

Es una preparación de hidróxido de magnesio en agua. Principalmente es una suspensión, por lo que debes agitar el frasco antes de consumirla (ya que el polvo se sedimenta). No obstante, las partículas más diminutas de la mezcla pueden permanecer flotando y comportarse temporalmente como un coloide, lo que le da su típico aspecto lechoso y opaco inconfundible.
3. Amoxicilina y Penicilina

En su presentación líquida (como la amoxicilina pediátrica o la penicilina inyectable benzatínica), estos antibióticos son suspensiones porque su principio activo es poco soluble. Por eso vienen en polvo para reconstituir y siempre deben agitarse vigorosamente antes de cada dosis. Se les añaden agentes espesantes (como la goma xantana o la celulosa microcristalina) que forman una red coloidal para evitar que el polvo decante demasiado rápido al fondo.
4. Barro o Arcilla en agua

Las partículas pesadas de tierra se hunden rápidamente al fondo del recipiente (suspensión). Sin embargo, las partículas de arcilla más finas quedan dispersas oscureciendo el agua y manteniéndola turbia por mucho tiempo (coloide).
5. Pinturas

Contienen pigmentos pesados que tienden a asentarse si se dejan reposar mucho tiempo (suspensión, se deben agitar antes de usar), pero están inmersos en un medio líquido de resinas y aglutinantes en estado coloidal.
6. Formulaciones de Insulina

La insulina regular es una solución verdadera (transparente y de acción rápida). En cambio, la insulina NPH (Neutral Protamine Hagedorn) es una suspensión intencional. Sus siglas indican que tiene un pH Neutro, contiene la proteína Protamina (que obliga a las moléculas a formar cristales insolubles para que se liberen lentamente en el cuerpo) y fue creada por Hans Hagedorn. Por tener estos cristales es turbia y siempre se debe mezclar frotando el frasco antes de usar.
Uso clínico: Un paciente diabético suele usar ambas. La solución (Regular) se inyecta con las comidas para bajar picos de azúcar de inmediato, mientras que la suspensión (NPH) proporciona un suministro lento y constante a lo largo del día y la noche, ya que el cuerpo tarda más tiempo en disolver sus cristales.
Sistemas Claramente Definidos
Para contrastar, aquí tienes ejemplos de mezclas de la vida diaria que pertenecen de forma mucho más estricta a una sola categoría:
Coloides Clásicos
- Mayonesa: Emulsión de aceite en agua estabilizada por la yema de huevo.
- Niebla / Neblina: Pequeñas gotas de agua líquida dispersas en un gas (el aire).
- Gelatina: Macromoléculas de proteína (colágeno) dispersas en agua caliente que luego se enfría.
- Espuma de afeitar: Gas disperso en un medio líquido.
- Piedra pómez: Burbujas de gas atrapadas en roca (espuma sólida).
Suspensiones Clásicas
- Agua con arena: Las partículas sólidas son enormes y se asientan casi de inmediato.
- Jugo de naranja natural: La pulpa de la fruta flota temporalmente pero termina en el fondo.
- Aderezos y vinagretas: El aceite, el vinagre y las especias se separan en capas al reposar.
- Antibióticos pediátricos: Polvos que se reconstituyen y deben agitarse vigorosamente antes de cada dosis.
- Refrescos naturales (horchata): Las partículas de los granos decantan en la base de la jarra.

Podcast: Sistemas Coloidales
Escucha la narración explicativa sobre los coloides, suspensiones y soluciones verdaderas.
Video Educativo: Coloides y Dispersiones
Presentación en PDF: Coloides y Dispersiones
Para mejor experiencia en celular, abre la guía directamente:
Abrir Presentación PDFVisualiza la Presentación.
Infografía: Coloides y Sistemas de Dispersión

- 1. Indique la diferencia principal, en términos de tamaño de partícula, entre una solución verdadera, un coloide y una suspensión.
- 2. ¿Qué es el Efecto Tyndall y por qué ocurre en los coloides y no en las soluciones verdaderas?
- 3. Mencione las dos partes o componentes fundamentales que conforman la anatomía de un sistema coloidal.
- 4. Si usted tiene una mezcla que pasa sin problemas por un filtro de papel ordinario, pero cuyas partículas son bloqueadas por una membrana celular semipermeable, ¿qué tipo de mezcla es?
- 5. Analizando la sangre humana desde el punto de vista fisicoquímico, describa los componentes que la convierten en una dispersión múltiple.
-
Discuta el papel fisiológico crucial de las proteínas coloidales en el plasma sanguíneo, haciendo énfasis en cómo su inmenso tamaño molecular previene la constante pérdida de líquidos del sistema circulatorio. Defina qué es la "presión oncótica" dentro de su postura.
-
Explique en qué consiste esencialmente un aparato de Hemodiálisis para un paciente con deficiencia renal crónica, fundamentándose exclusivamente en los principios de barreras químicas, diámetros de poro microscópicos (filtro en laboratorio), y las soluciones endovenosas.
-
Utilizando el "Simulador de Efecto Tyndall" y el de "Membranas" vistos anteriormente, elabore un contraste mental entre los tres estados. Si tuviera que crear un "experimento casero" para enseñarle el Efecto Tyndall a un menor, ¿qué objetos usaría y qué fluido no lograria dar efecto?