Instrucciones
Usted tiene las siguientes opciones en este simulador para moléculas pequeñas tanto inorgánicas como orgánicas.
- En la parte superior, aparecen los botones 2D y 3D para que pueda observar el modelo en dos o tres dimensiones.
- A continuación se presenta el modelo en dos o tres dimensiones.
- "Search" puede ser utilizado para buscar alguna molécula, escribiendo el nombre en inglés, por ejemplo al escribir, sulphuric acid (ácido sulfúrico).
- Color de fondo, sirve seleccionar el color del fondo del modelo en tres dimensiones.
- Acercar +, acerca el modelo.
- Acercar -, aleja el modelo.
- Girar X, Y, Z, para girar el modelo en tres dimensiones en los ejes x, y, z.
- Alambres, varillas y pelotas y varillas, para cambiar el modelo en tres dimensiones en esas representaciones.
- Energía, aparce en la parte superior la energía de la molécula en kJ/mol o kcal/mol.
- Minmizar por MMFF94, normalmente las estructuras iniciales que se crean en los simuladores poseen energías mucho mayores a las que tendría un objeto real, por esta razón, se utilizan algoritmos para calcular las posiciones y fuerzas originales, con el objetivo de minimizarlas y que sean más realistas.
- Arrastrar Minimizar, usted puede arrastrar un átomo, soltarlo y entonces el sistema hace un cálculo de minimización de energía.
- Simetría, muestra los planos de simetría en la molécula.
- Editar, puede editar la molécula agragando o quitando átomos y enlaces.
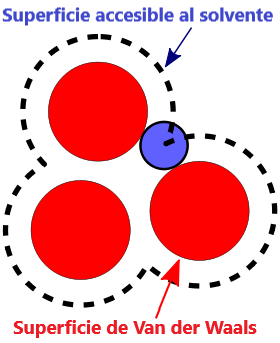
- Superficie VDW, la superficie de van der Waals de una molécula es una representación abstracta o modelo de esa molécula, que ilustra dónde, en términos muy generales, podría haber una superficie para la molécula en función de los cortes duros de los radios de van der Waals para átomos individuales, y representa una superficie a través de la cual la molécula podría concebirse interactuando con otras moléculas.
- PEM es el mapa de potencial electrostático.
- Carga parcial calcula la carga parcial de cada átomo.
- Tetraedros, para el caso que exista alguna átomo tetraédrico.
- Dipolos enlaces, para ver el los dipolos de todos los enlaces.
- Dipolo molecular, para ver el momento dipolar resultante de toda la molécula.
- Hibridación sp, sp2 y sp3, para ver la hibridacion del átomo de carbono.
- Anillo aromático, muestra los anillos aromáticos.
- Heteroátomo, muestra los heteroátomos en heterociclos.
- C quiral (nomenclatura R/S) y E/Z para isomería geométrica en alquenos, los descriptores R/S permiten indicar en un compuesto orgánico la configuración (la disposición espacial de los sustituyentes) de un carbono o centro quiral, estereocentro o centro estereogénico, que es el caso de un átomo de carbono con cuatro sustituyentes diferentes. Se añade R o S entre paréntesis como prefijo delante del nombre de la molécula orgánica. En caso de ser más de uno el centro estereogénico, separados por coma se indica el descriptor R o S de cada uno, precedido del número o localizador que identifica su posición.
- Invertir R/S, para cambiar la quiralidad.
- Nomenclatura E/Z en Alquenos, el sistema tradicional para nombrar los isómeros geométricos de un alqueno, en el que los mismos grupos están dispuestos de manera diferente, es nombrarlos como cis o trans. Sin embargo, es fácil encontrar ejemplos donde el sistema cis-trans no se aplica fácilmente.
- N electrones, O electrones y S electrones, para ver los electrones libres del nitrógeno, oxígeno y azufre.
- C primario, C secundario, C terciario, C cuaternario, identifica la clasificación de los átomos de carbono.
- Dadores y aceptores de puentes de hidrógeno, señala los átomos que pueden dar o aceptar puentes de hidrógeno
- Botón 2D, cuando escoge el botón 2D, la aplicación tiene su propio menú y quedan inhabilitados todos los botones 3D.<
Laboratorio de IA: Tu Copiloto de Estudio
Aprende a usar la Inteligencia Artificial Científica
La IA no sirve solo para dar respuestas, sino para profundizar el pensamiento hipotético, clínico y matemático. Aquí tienes 6 prompts diseñados para trabajar exactamente los temas de esta hoja: osmolaridad, tonicidad, efecto sobre eritrocitos, ejercicios de membrana y uso clínico de soluciones.
1. Conceptos Fundamentales
Osmolaridad, tonicidad e isoosmolaridad.
2. Cálculo de Osmolaridad
Aplicación de i × C.
3. Eritrocito y Tonicidad
Hemólisis, isotonicidad y crenación.
4. Membrana Semipermeable
Dirección del agua en sistemas A y B.
5. Solutos y Movimiento
Agua, acetona y glicerol.
6. Aplicación Clínica
NaCl 3%, agua destilada y seguridad IV.
Coloides
Osmolaridad
Definición: Es la concentración de partículas osmóticamente activas disueltas en una solución, expresada en osmoles por litro (osm/L).
Fórmula:
Osmolaridad = i × C
donde:
i = factor de disociación (número de partículas)
C = concentración molar de la solución
Característica clave: Es una propiedad coligativa que depende SOLO del número de partículas, no de su naturaleza química.
Valor normal en plasma: 280-300 mOsm/L
Tonicidad
Definición: Es la capacidad de una solución para cambiar el volumen de una célula al compararla con el plasma, dependiendo de las sustancias que pueden cruzar la membrana.
Punto crítico: NO todas las sustancias osmóticamente activas contribuyen a la tonicidad. Solo las sustancias que NO pueden cruzar la membrana plasmática generan presión osmótica efectiva.
Valor normal en plasma: Isotónico (0.3 osm/L de solutos impermeables)
Comparación: Osmolaridad vs Tonicidad
| Característica | Osmolaridad | Tonicidad |
|---|---|---|
| ¿Qué mide? | Concentración total de partículas disueltas | Capacidad de cambiar volumen celular |
| ¿Qué importa? | Número total de partículas (A + B + C) | Solo partículas que NO cruzan membrana |
| Método | Físico (congelación, presión osmótica) | Observación del efecto celular |
| Ejemplo paradoja | Glucosa 5% aporta osmolaridad al inicio | La glucosa entra y se metaboliza; por eso no mantiene tonicidad efectiva y puede terminar como hipotónica |
| Aplicación clínica | Diagnóstico de hiponatremia/hipernatremia | Selección de fluidos IV seguros |
Tabla de Tonicidad y Osmolaridad
| Tonicidad | Valor de osmolaridad | Concentración de solutos, respecto a los que hay en el interior de una célula. Ej. Eritrocito | Efecto en la célula (ej. Eritrocito) al ser introducida en esta solución |
|---|---|---|---|
| Hipotónica | < 0.28 | Posee menor concentración de solutos, de los que hay en el interior de la célula. | Entra agua al eritrocito, éste se hincha y explota, hay hemólisis. |
| Isotónica | 0.28 - 0.32 | Posee la misma concentración de solutos, de las que hay en el interior de la célula. | Conserva su volumen; no se afecta su morfología. |
| Hipertónica | > 0.32 | Posee mayor concentración de solutos de los que hay en el interior de la célula. | Sale agua del eritrocito, se encoge. Hay crenación. |
| *En isotónica, entra y sale agua del eritrocito a la misma velocidad, por eso no es afectada su morfología. | |||
Clasificación de Soluciones según Tonicidad
Soluciones Isotónicas
Osmolaridad: = plasma (0.3 osm/L)
Efecto en células: Sin cambio de volumen
Ejemplos clínicos:
- NaCl 0.9%
- Glucosa 5%: inicialmente cercana a isotónica, pero luego puede comportarse como hipotónica
- Lactato de Ringer
- Plasma normal
Uso clínico: Seguras para infusión IV prolongada
Soluciones Hipertónicas
Osmolaridad: > plasma (> 0.3 osm/L)
Efecto en células: Crenación (encogimiento)
Ejemplos clínicos:
- NaCl 3-7.5%
- Glucosa 10-50%
- Dextrano hipertónico
Uso clínico: Edema cerebral, hiperhidratación
Soluciones Hipotónicas
Osmolaridad: < plasma (< 0.3 osm/L)
Efecto en células: Hemólisis (estallido)
Ejemplos clínicos:
- NaCl 0.45%
- Agua destilada
- Glucosa 2.5%
Uso clínico: PELIGRO: Riesgo de edema cerebral
Videos: Soluciones Isotónicas, Hipotónicas e Hipertónicas
Isotónica
Hipotónica
Hipertónica
Ejemplo 1: Cálculo de Osmolaridad
Pregunta: ¿Cuál es la osmolaridad de una solución de NaCl 0.25 M?
Ionización
NaCl H₂O⟶ Na+ + Cl−
(se forma dos iones)
Respuesta
El NaCl se ioniza completamente formando dos iones
Osmolaridad = 0.25 × 2 = 0.5 osmolar
Ejemplo 2: Cálculo de Osmolaridad
Pregunta: ¿Cuál es la osmolaridad de una solución de K2SO4 0.5 M?
Ionización
K2SO4 H₂O⟶ 2K+ + SO42−
(se forma tres iones)
Respuesta
El K2SO4 se ioniza totalmente formando tres iones
Osmolaridad = 0.5 × 3 = 1.5 osmolar
Ejemplo 3: Cálculo de Osmolaridad
Pregunta: ¿Cuál es la osmolaridad de una solución de MgCl2 0.10 M?
Ionización
MgCl2 H₂O⟶ Mg2+ + 2Cl−
(se forma tres iones)
Respuesta
El MgCl2 se ioniza totalmente formando tres iones
Osmolaridad = 0.10 × 3 = 0.30 osmolar
Ejemplo 4: Cálculo de Osmolaridad
Pregunta: ¿Cuál es la osmolaridad de una solución de glucosa 1.0 M?
Ionización
Glucosa H₂O⟶ Glucosa (no se ioniza)
(solo una partícula en solución)
Respuesta
La glucosa no se ioniza en solución acuosa
Osmolaridad = 1.0 × 1 = 1.0 osmolar
Ejemplo 5: Cálculo de Osmolaridad
Pregunta: ¿Cuál es la osmolaridad de una solución de NaCl 0.9% (≈ 0.15 M)?
Ionización
NaCl H₂O⟶ Na+ + Cl−
(se forma dos iones)
Cálculo de molaridad por factor unitario:
| 0.90 g NaCl | × | 1000 mL | × | 1 mol NaCl |
| 100 mL | 1 L | 58.44 g NaCl |
= 0.15 M
Respuesta
El NaCl se ioniza completamente formando dos iones
Osmolaridad = 0.15 × 2 = 0.30 osmolar
Ejercicios: ¿Hacia dónde se desplaza el agua?
Sistema A (izquierda) y B (derecha)
Observe el sistema y resuelva de uno en uno hacia qué lado se mueve el agua por ósmosis.

Sistema de referencia: compartimiento A (izquierda) y B (derecha).
a) A: 1% glucosa | B: 5% glucosa
b) A: 0.1 M glucosa | B: 0.5 M glucosa
c) A: 1 M NaCl | B: 1 M glucosa
d) A: 1 M NaCl | B: 1 M K2SO4
e) A: 3% NaCl | B: 3% KCl
f) A: 1 M NaBr | B: 1 M KCl
g) En el sistema 2, A: NaCl 0.9 % p/v y B: NaCl 3 M. ¿Hacia donde se desplaza el agua?

h) En el sistema 3, A: 0.15 M (urea) + 0.3 M (proteína) y B: 3 M (urea) + 0.6 M (proteína). ¿Hacia dónde se desplaza el agua?

i) En el sistema 4, A: acetona 7 % + glicerol 0.3 % y B: acetona 3 % + glicerol 0.3 %. ¿Hacia dónde se desplazan el agua y los solutos?

Aplicaciones Clínicas en Medicina
Casos clínicos importantes:
- Deshidratación (Hipernatremia): Se administran soluciones hipotónicas gradualmente para evitar edema cerebral mientras se rehidrata.
- Edema cerebral (Hemorragia intracraneal): Se usan soluciones hipertónicas (NaCl 3% o hiperglucemias) para crear gradiente osmótico que reduzca presión intracraneal.
- Transfusión de sangre: Los glóbulos rojos deben mantenerse en solución isotónica para evitar hemólisis o crenación.
- Hidratación perioperatoria: Solo composiciones isotónicas (Ringer, NaCl 0.9%) pueden infundirse sostenidamente sin riesgo.
- Manejo de quemaduras: Fórmula de Parkland: LR isotónico 4 mL × peso (kg) × % quemadura, distribuido en 24 h.
⚠️ Errores frecuentes en clínica:
- Confundir "isoosmótica" con "isotónica" - pueden ser diferentes
- Infundir soluciones ipotónicas rápidamente causando edema celular
- No considerar que la glucosa se metaboliza y pierde tonicidad efectiva con el tiempo
- Olvidar monitorizar osmolaridad sérica en el paciente, no solo de la solución

Podcast: Tonicidad
Escucha la narración explicativa sobre los conceptos de tonicidad.
Video Educativo: Tonicidad
Presentación en PDF: Tonicidad
Para mejor experiencia en celular, abre la guía directamente:
Abrir Presentación PDFVisualiza la Presentación.
Infografía: Tonicidad
(Imagen pendiente de agregar al servidor)

Instrucciones
Responda primero con sus propias palabras y luego verifique con la Guía PDF, la calculadora de osmolaridad y los ejercicios de la página.
- 1. ¿Cuál es la diferencia esencial entre osmolaridad y tonicidad?
- 2. ¿Cuál es la fórmula básica para calcular la osmolaridad de una solución?
- 3. ¿Cuál es el valor normal aproximado de la osmolaridad plasmática?
- 4. ¿Por qué una solución puede ser isoosmótica pero no isotónica?
- 5. ¿Qué ocurre con un eritrocito en una solución hipotónica, isotónica e hipertónica?
- 6. ¿Cuál es la osmolaridad de NaCl 0.25 M?
- 7. ¿Cuál es la osmolaridad de K2SO4 0.5 M?
- 8. ¿Cuál es la osmolaridad de MgCl2 0.10 M?
- 9. ¿Cuál es la osmolaridad de glucosa 1.0 M?
- 10. ¿Qué representa el factor i y cómo cambia entre NaCl y glucosa al calcular osmolaridad?
-
Explique detalladamente la diferencia entre osmolaridad y tonicidad, y por qué esta distinción es importante en fisiología y medicina.
-
Explique por qué NaCl 0.9% y glucosa 5% aparecen como ejemplos clínicos importantes en esta hoja y cómo se relacionan con la isotonicidad.
-
Una enfermera administra por error una solución de NaCl al 3%. Analice el efecto esperado sobre los eritrocitos del paciente.
-
Resuelva el sistema 3 de la guía de ejercicios: A = 0.15 M urea + 0.3 M proteína; B = 3 M urea + 0.6 M proteína. Indique hacia dónde se mueve el agua según el planteamiento del material.
-
Analice el sistema 4 con acetona y glicerol: indique la dirección del agua, de la acetona y del glicerol.
Medicina Hospitalaria:
- NaCl 0.9%: Mantiene volumen intravascular sin hemólisis ni crenación.
- NaCl 3%: Se reserva para indicaciones específicas como edema cerebral; no es una solución de mantenimiento general.
- Agua destilada: No debe administrarse IV por el alto riesgo de hemólisis.
Razonamiento Clínico:
- Hemólisis: Ocurre en medios hipotónicos por entrada excesiva de agua.
- Crenación: Ocurre en medios hipertónicos por pérdida de agua celular.
- Calculadora y simulador: Ayudan a predecir el efecto de una solución antes de aplicarla.
Ruta Recomendada de Estudio
1. Revise las definiciones de osmolaridad y tonicidad.
2. Practique los ejemplos de cálculo de osmolaridad.
3. Resuelva los ejercicios de desplazamiento de agua antes de ver la respuesta.
4. Compruebe su razonamiento con el simulador y la calculadora de la página.
Reto Rápido
Clasifique y justifique: NaCl 0.9%, NaCl 2%, glucosa 1% y glucosa 5%.
Pista: calcule primero la osmolaridad y luego relacione el resultado con el efecto sobre el eritrocito.