Instrucciones
Usted tiene las siguientes opciones en este simulador para moléculas pequeñas tanto inorgánicas como orgánicas.
- En la parte superior, aparecen los botones 2D y 3D para que pueda observar el modelo en dos o tres dimensiones.
- A continuación se presenta el modelo en dos o tres dimensiones.
- "Search" puede ser utilizado para buscar alguna molécula, escribiendo el nombre en inglés, por ejemplo al escribir, sulphuric acid (ácido sulfúrico).
- Color de fondo, sirve seleccionar el color del fondo del modelo en tres dimensiones.
- Girar X, Y, Z, para girar el modelo en tres dimensiones en los ejes x, y, z.
- Alambres, varillas y pelotas y varillas, para cambiar el modelo en tres dimensiones en esas representaciones.
- Energía, aparce en la parte superior la energía de la molécula en kJ/mol o kcal/mol.
- Minmizar por MMFF94, normalmente las estructuras iniciales que se crean en los simuladores poseen energías mucho mayores a las que tendría un objeto real, por esta razón, se utilizan algoritmos para calcular las posiciones y fuerzas originales, con el objetivo de minimizarlas y que sean más realistas.
- Arrastrar Minimizar, usted puede arrastrar un átomo, soltarlo y entonces el sistema hace un cálculo de minimización de energía.
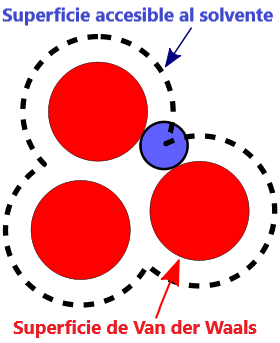
- Superficie VDW, La superficie de van der Waals de una molécula es una representación abstracta o modelo de esa molécula, que ilustra dónde, en términos muy generales, podría haber una superficie para la molécula en función de los cortes duros de los radios de van der Waals para átomos individuales, y representa una superficie a través de la cual la molécula podría concebirse interactuando con otras moléculas.
- PEM es el mapa de potencial electrostático.
- Cargas parciales, para ver el valor de la carga relativa positiva o negativa de cada átomo.
- Tetraedros, para el caso que exista alguna átomo tetraédrico.
- Dipolos enlaces, para ver el los dipolos de todos los enlaces.
- Dipolo molecular, para ver el momento dipolar resultante de toda la molécula.
- Botón 2D, cuando escoge el botón 2D, la aplicación tiene su propio menú y quedan inhabilitados todos los botones 3D.
Equilibrio Químico
Ejercicios de Química Constante de Equilibrio
¡Bienvenidos, estudiantes!
En esta guía interactiva encontrarán una serie de ejercicios diseñados para practicar el planteamiento y cálculo de la constante de equilibrio (\(\text{K}_{\text{eq}}\)). Podrán verificar sus respuestas paso a paso expandiendo las soluciones.
Herramienta de apoyo: En la esquina inferior derecha de su pantalla encontrarán un botón flotante azul. Al hacer clic en él, tendrán acceso inmediato a nuestro Analizador de Equilibrio Químico. Utilicen esta calculadora para escribir sus ecuaciones, practicar el balanceo estequiométrico y comprobar sus resultados analíticos.
Ejercicio 1
¿Cuál es la constante de equilibrio para la siguiente reacción?
Respuesta:
Ejercicio 2
¿Cuál es la constante de equilibrio para la siguiente reacción?
Respuesta:
Ejercicio 3
¿Cuál es la constante de equilibrio para la siguiente reacción?
Respuesta:
Ejercicio 4
¿Cuál es la constante de equilibrio para la siguiente reacción?
Respuesta:
Ejercicio 5
¿Cuál es la constante de equilibrio para la siguiente reacción si las concentraciones en el equilibrio son \([\text{SO}_2]=0.55\text{ M}\); \([\text{H}_2\text{O}]=0.25\text{ M}\); \([\text{H}_2\text{S}]=0.60\text{ M}\); \([\text{O}_2]=0.10\text{ M}\)?
Respuesta:
Ejercicio 6
¿Cuál es la \([\text{N}_2\text{O}_4]\) si \(\text{K}_{\text{eq}}\) para la reacción es 0.211 y la concentración en el equilibrio de \([\text{NO}_2]=0.25\text{ M}\)?
Respuesta:
$$ [\text{N}_2\text{O}_4] = \frac{[\text{NO}_2]^2}{\text{K}_{\text{eq}}} = \frac{[0.25]^2}{0.211} = 0.30\text{ M} $$
Ejercicio 7 (Equilibrio Homogéneo)
¿Cuál es la constante de equilibrio para la síntesis del amoníaco si las concentraciones en el equilibrio son \([\text{N}_2]=0.10\text{ M}\), \([\text{H}_2]=0.10\text{ M}\) y \([\text{NH}_3]=0.20\text{ M}\)?
Respuesta:
Ejercicio 8 (Equilibrio Heterogéneo)
¿Cuál es la concentración de \(\text{CO}_2\) en el equilibrio si la \(\text{K}_{\text{eq}}\) para la descomposición del carbonato de calcio es \(0.050\)?
Respuesta:
$$ [\text{CO}_2] = 0.050\text{ M} $$
Ejercicio 9 (Equilibrio Homogéneo)
Encuentre la concentración en el equilibrio del yoduro de hidrógeno \([\text{HI}]\) si \(\text{K}_{\text{eq}} = 50.0\), y las concentraciones de los reactivos son \([\text{H}_2]=0.20\text{ M}\) e \([\text{I}_2]=0.20\text{ M}\).
Respuesta:
$$ [\text{HI}] = \sqrt{50.0 \times 0.040} = 1.41\text{ M} $$
Ejercicio 10 (Equilibrio Heterogéneo)
Calcule la constante de equilibrio de la reacción del carbono sólido con vapor de agua si \([\text{H}_2\text{O}]=0.10\text{ M}\), \([\text{CO}]=0.20\text{ M}\) y \([\text{H}_2]=0.20\text{ M}\).
Respuesta:
Ejercicio 11 (Equilibrio Homogéneo)
Calcule la \(\text{K}_{\text{eq}}\) para la síntesis de metanol gaseoso si las concentraciones en el equilibrio son \([\text{CO}]=0.50\text{ M}\), \([\text{H}_2]=0.20\text{ M}\) y \([\text{CH}_3\text{OH}]=0.15\text{ M}\).
Respuesta:
Ejercicio 12 (Equilibrio Heterogéneo)
El hidrógenosulfuro de amonio sólido se descompone en gases. Si \(\text{K}_{\text{eq}} = 0.16\) y \([\text{NH}_3]=0.40\text{ M}\), ¿cuál es la concentration de \(\text{H}_2\text{S}\)?
Respuesta:
$$ [\text{H}_2\text{S}] = \frac{0.16}{0.40} = 0.40\text{ M} $$
Ejercicio 13 (Equilibrio Homogéneo)
Calcule la concentración de \(\text{PCl}_3\) sabiendo que \(\text{K}_{\text{eq}} = 0.025\), \([\text{PCl}_5]=0.10\text{ M}\) y \([\text{Cl}_2]=0.050\text{ M}\).
Respuesta:
$$ [\text{PCl}_3] = \frac{0.025 \times 0.10}{0.050} = 0.050\text{ M} $$
Ejercicio 14 (Equilibrio Heterogéneo)
Calcule la \(\text{K}_{\text{eq}}\) para la formación de níquel tetracarbonilo si \([\text{CO}]=0.50\text{ M}\) y \([\text{Ni(CO)}_4]=0.25\text{ M}\).
Respuesta:
Ejercicio 15 (Equilibrio Homogéneo)
¿Cuál es la \(\text{K}_{\text{eq}}\) de la reacción de oxidación si \([\text{NO}]=0.020\text{ M}\), \([\text{O}_2]=0.010\text{ M}\) y \([\text{NO}_2]=0.040\text{ M}\)?
Respuesta:
Ejercicio 16 (Equilibrio Heterogéneo)
Calcule la concentración de monóxido de carbono \([\text{CO}]\) si \(\text{K}_{\text{eq}} = 1.5\) y \([\text{CO}_2]=0.60\text{ M}\).
Respuesta:
$$ [\text{CO}] = \sqrt{1.5 \times 0.60} = 0.95\text{ M} $$
Ejercicio 17 (Combustión Gaseosa a Alta Temperatura)
La combustión del propano en el interior de un horno industrial ocurre a temperaturas tan altas que los gases de escape establecen un equilibrio térmico con un valor de \(\text{K}_{\text{eq}} = 86.4\). Si se analizan los gases y se encuentran las siguientes concentraciones: \([\text{C}_3\text{H}_8]=0.050\text{ M}\), \([\text{O}_2]=0.10\text{ M}\) y \([\text{H}_2\text{O}]=0.20\text{ M}\), calcule la concentración del dióxido de carbono \([\text{CO}_2]\).
Respuesta paso a paso:
$$ 86.4 = \frac{[\text{CO}_2]^3 [0.20]^4}{[0.050] [0.10]^5} $$
$$ 86.4 = \frac{[\text{CO}_2]^3 (1.6 \times 10^{-3})}{(0.050) (1.0 \times 10^{-5})} $$
$$ 86.4 = \frac{[\text{CO}_2]^3 (1.6 \times 10^{-3})}{5.0 \times 10^{-7}} $$
$$ [\text{CO}_2]^3 = \frac{86.4 \times (5.0 \times 10^{-7})}{1.6 \times 10^{-3}} = \frac{4.32 \times 10^{-5}}{1.6 \times 10^{-3}} = 0.027 $$
$$ [\text{CO}_2] = \sqrt[3]{0.027} = 0.30\text{ M} $$