Instrucciones
Usted tiene las siguientes opciones en este simulador para moléculas pequeñas tanto inorgánicas como orgánicas.
- En la parte superior, aparecen los botones 2D y 3D para que pueda observar el modelo en dos o tres dimensiones.
- A continuación se presenta el modelo en dos o tres dimensiones.
- "Search" puede ser utilizado para buscar alguna molécula, escribiendo el nombre en inglés, por ejemplo al escribir, sulphuric acid (ácido sulfúrico).
- Color de fondo, sirve seleccionar el color del fondo del modelo en tres dimensiones.
- Acercar +, acerca el modelo.
- Acercar -, aleja el modelo.
- Girar X, Y, Z, para girar el modelo en tres dimensiones en los ejes x, y, z.
- Alambres, varillas y pelotas y varillas, para cambiar el modelo en tres dimensiones en esas representaciones.
- Energía, aparce en la parte superior la energía de la molécula en kJ/mol o kcal/mol.
- Minmizar por MMFF94, normalmente las estructuras iniciales que se crean en los simuladores poseen energías mucho mayores a las que tendría un objeto real, por esta razón, se utilizan algoritmos para calcular las posiciones y fuerzas originales, con el objetivo de minimizarlas y que sean más realistas.
- Arrastrar Minimizar, usted puede arrastrar un átomo, soltarlo y entonces el sistema hace un cálculo de minimización de energía.
- Simetría, muestra los planos de simetría en la molécula.
- Editar, puede editar la molécula agragando o quitando átomos y enlaces.
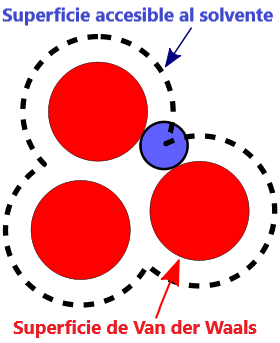
- Superficie VDW, la superficie de van der Waals de una molécula es una representación abstracta o modelo de esa molécula, que ilustra dónde, en términos muy generales, podría haber una superficie para la molécula en función de los cortes duros de los radios de van der Waals para átomos individuales, y representa una superficie a través de la cual la molécula podría concebirse interactuando con otras moléculas.
- PEM es el mapa de potencial electrostático.
- Carga parcial calcula la carga parcial de cada átomo.
- Tetraedros, para el caso que exista alguna átomo tetraédrico.
- Dipolos enlaces, para ver el los dipolos de todos los enlaces.
- Dipolo molecular, para ver el momento dipolar resultante de toda la molécula.
- Hibridación sp, sp2 y sp3, para ver la hibridacion del átomo de carbono.
- Anillo aromático, muestra los anillos aromáticos.
- Heteroátomo, muestra los heteroátomos en heterociclos.
- C quiral (nomenclatura R/S) y E/Z para isomería geométrica en alquenos, los descriptores R/S permiten indicar en un compuesto orgánico la configuración (la disposición espacial de los sustituyentes) de un carbono o centro quiral, estereocentro o centro estereogénico, que es el caso de un átomo de carbono con cuatro sustituyentes diferentes. Se añade R o S entre paréntesis como prefijo delante del nombre de la molécula orgánica. En caso de ser más de uno el centro estereogénico, separados por coma se indica el descriptor R o S de cada uno, precedido del número o localizador que identifica su posición.
- Invertir R/S, para cambiar la quiralidad.
- Nomenclatura E/Z en Alquenos, el sistema tradicional para nombrar los isómeros geométricos de un alqueno, en el que los mismos grupos están dispuestos de manera diferente, es nombrarlos como cis o trans. Sin embargo, es fácil encontrar ejemplos donde el sistema cis-trans no se aplica fácilmente.
- N electrones, O electrones y S electrones, para ver los electrones libres del nitrógeno, oxígeno y azufre.
- C primario, C secundario, C terciario, C cuaternario, identifica la clasificación de los átomos de carbono.
- Dadores y aceptores de puentes de hidrógeno, señala los átomos que pueden dar o aceptar puentes de hidrógeno
- Botón 2D, cuando escoge el botón 2D, la aplicación tiene su propio menú y quedan inhabilitados todos los botones 3D.
Laboratorio de IA: Tu Copiloto de Estudio
Aprende a usar la Inteligencia Artificial Científica
La IA no sirve solo para dar respuestas, sino para profundizar el razonamiento químico, clínico y matemático. Si estudias equilibrio químico, aquí tienes 6 "Prompts" avanzados para desafiar tu comprensión analítica de la espontaneidad, la energía libre y el equilibrio dinámico:
1. Cinética vs. Termodinámica
Velocidad de reacción y dirección espontánea.
2. Energía Libre de Gibbs
Interpretación física de ΔG.
3. Aplicación Clínica del BaSO4
Solubilidad, toxicidad y uso médico.
4. Energía de Activación
Barreras energéticas y perfil de reacción.
5. Equilibrio Dinámico
Velocidades opuestas y estado final.
6. Autoevaluación Guiada
Repaso socrático de equilibrio químico.
Equilibrio Químico
De acuerdo con los cálculos, el carbono en la forma de debería transformarse espontáneamente en . Sin embargo, los dueños de diamantes no se preocupan por perder sus gemas, porque esa transformación ocurre de manera extraordinariamente lenta. Este ejemplo muestra a estudiantes de ciencias médicas y de física-matemática una idea clave de la cinética: una reacción puede ser favorable termodinámicamente y, aun así, avanzar a una velocidad tan baja que resulte imperceptible.
Por otra parte, el bario, en forma de iones Ba2+, es muy venenoso. Cuando el (BaSO4) se disuelve, se forman acuosos. A pesar de ello, suspensiones de BaSO4 sólido se usan rutinariamente en medicina para estudios radiológicos del tracto digestivo. Los pacientes no sufren daño sistémico porque solo una cantidad infinitesimal del sólido se disuelve: el equilibrio entre el BaSO4 sólido y sus iones está fuertemente desplazado en favor de la forma sólida protectora.
De esto desprendemos una premisa clínica y técnica fundamental: Mientras que el diamante nos muestra que la cinética dicta la velocidad de un proceso, el sulfato de bario nos demuestra que la termodinámica dicta en qué dirección ocurre. El equilibrio químico es el estado final donde estas dos fuerzas logran un balance íntegro.
Procesos espontáneos y no espontáneos
Hace varios años, los turistas visitaban la "colina de la gravedad" en la ciudad de Salt Lake, donde una ilusión óptica hacía parecer que una corriente de agua fluía cuesta arriba. La fascinación por la escena surgía de la aparente violación de las leyes naturales. Los procesos que se llevan a cabo por sí mismos, sin una intervención continua, se llaman procesos espontáneos. Los procesos no espontáneos ocurren solo cuando reciben una causa o un estímulo externo. Esta analogía con una piedra sobre una colina ayuda a visualizar tres situaciones químicas distintas.

Colina de la Gravedad en la ciudad de Salt Lake, Estados Unidos
En la situación A de nuestro símil mecánico, la piedra rodará hacia abajo tan pronto como usted la suelte; el proceso inicia y continúa espontáneamente. En la situación B, mecánicamente debe darle un pequeño empujón inicial para vencer el obstáculo inicial en el trayecto, pero una vez superado este contratiempo, la dinámica manda y la piedra cae por sí sola hacia una hondonada prolongada. En la situación C, el escenario dictaminado es muy diferente: el estudiante debe empujar continuamente la pesada piedra con trabajo de la musculatura o esta indudablemente ya no se moverá ninguna pulgada cuesta arriba. El proceso de subida es obligatoriamente NO espontáneo y ocurre pura y exclusivamente mientras se aplique activamente la potencia de ese estímulo externo.
Fundamento de Energía Libre para interpretar A, B y C
En el simulador, la altura de la colina representa de forma cualitativa la energía libre de Gibbs (G). Lo importante no es solo si existe un obstáculo, sino cómo cambia la energía libre entre el punto inicial y el final del proceso, es decir, el signo de ΔG.
- Situación A: la piedra termina más abajo que al inicio. Eso significa que el sistema pasa a un estado de menor energía libre, por lo que ΔG < 0. El proceso es espontáneo o exergónico.
- Situación B: al principio hay una pequeña subida, pero el punto final también queda más abajo que el inicial. En consecuencia, el proceso sigue teniendo ΔG < 0 y es espontáneo en términos termodinámicos, aunque necesita primero vencer una barrera de activación. Esa subida inicial es la analogía de la energía de activación (Ea).
- Situación C: la piedra solo puede avanzar si se le empuja continuamente hacia una región más alta. El estado final queda con mayor energía libre que el inicial, por lo que ΔG > 0. El proceso es no espontáneo o endergónico.
La clave didáctica es esta: la espontaneidad la decide ΔG, mientras que la rapidez con la que algo ocurre depende de la energía de activación. Por eso una reacción puede ser espontánea y aun así avanzar muy lentamente, como sucede en la situación B y como ocurre en muchos procesos químicos reales.
Frecuentemente se pierde el máximo potencial aplicable de esta maravilla mecánica al no transfigurarse directamente de vuelta al contexto de una colisión química real. Podemos mapear por completo cada escenario directamente hacia variables biológicas y fisicomatemáticas conocidas:
- Situación A (Reacción espontánea sin estímulo perenne): Es equivalente al proceso donde entra en juego la difusión de una simple gota de tinta dispersante en el agua en un receptáculo que ocurre sin estímulo alguno adicional, tal y cual un flujo simple del cuerpo de nutrientes de donde la biomasa presenta más hacia donde ostenta deficiencias (ej. permeabilidad cruzada de iones biológicos). Sencillamente evoluciona espontáneamente cruzando gradientes para maximizar su desorden físico (entropía).
- Situación B (El "empujón inicial" para que opere libremente post ignición): Coincide nítidamente con la noción universal de la energía de activación; esto se asemeja diametralmente por ejemplo a contemplar la combustión química general producida por la quema de un trozo de madera o azúcar celular: la chispa desatada que lo inflama funciona como aquel "pequeño empujón", una vez que se activa, el trozo ya arderá en llamas ardiendo de manera autosuficiente espontáneamente para liberar un fulgurante resplandor termodinámico y calor exotérmico constante sin volver a exigir del empujador primario.
- Situación C (Un proceso forzado, no espontáneo que requiere suministro perenne): Ejemplifica y muestra casos analógicos a una recarga de su batería celular conectada a la toma eléctrica, un respirador clínico continuo, la reactivación forzada de una pila industrial o los flujos controlados desde la misma electrolisis forzada de las aguas purificadas. Tan claro como se interrumpe el enchufe (y paras de empujar momentáneamente la "piedra"), del todo la progresión del recargado detiene sus compuertas inversoras e interrumpe radical y repentinamente el flujo final de reacciones de carga en curso cayendo reverso.
Visto desde la ecuación de Gibbs, el simulador enseña una diferencia decisiva entre termodinámica y cinética:
ΔG = ΔH - TΔS
Energía Libre
dictamina la Espontaneidad
Entalpía
representa el Calor liberado/absorbido
Temperatura × Entropía
representa la Dispersión y Desorden
La termodinámica responde si el cambio es favorable en conjunto mediante el signo de ΔG, mientras que la cinética responde qué tan difícil es iniciar la transformación mediante la barrera de activación. Así, el estudiante no debe confundir “hay una subida inicial” con “el proceso no es espontáneo”: esa subida puede representar solo el costo inicial para activar una reacción cuyo balance global sigue siendo favorable.

Conforme la piedra rueda hacia abajo, libera energía y pasa de un estado de mayor energía potencial a uno de menor energía. Conforme usted la empuja hacia arriba, la piedra gana energía. Los procesos que liberan energía se denominan exergónicos, mientras que los que requieren energía se denominan endergónicos. Con mucha frecuencia, esos cambios energéticos aparecen como intercambio de calor; en ese caso, hablamos de procesos exotérmicos cuando liberan calor y endotérmicos cuando lo absorben.
Simulador interactivo disponible
Abra el laboratorio virtual de cinética y termodinámica desde el banner superior o desde el botón flotante para analizar espontaneidad, entropía y energía libre sin interrumpir la lectura del contenido.
A pesar de esta lógica que empareja energía con actividad, no todos los procesos pueden ser resumidos con el perfil único de una caída de su energía exotérmica para ocurrir sin obstáculos. La espontaneidad exige observar rigurosamente la otra variante decisiva en gran escala del universo: un incremento notable en su inmensidad dispersora, es la famosa y poderosa Entropía del estado macroscópico molecular dispersante y microscópico.
Como síntesis de las disyuntivas previas en nuestro análisis académico integral: La espontaneidad es un claro tira y afloja en la naturaleza.
Por un lado, frente a frente compitiendo se posicionan sistemas biológicos y energéticos orgánicos donde por su naturaleza de enlaces quieren fundamentalmente buscar la menor expresión energética posible; por ello, siempre quieren perder y liberar su energía disipándola (siendo exotérmicos preferiblemente).
Por el extremo recíproco y radical opuesto, compite en la balanza inmensamente su avidez espacial, deseando con voracidad e impaciencia acrecentar en la mejor capacidad que puedan el aumento contundente del desorden en toda regla en su posición macroscópica de materia usando la entropía para ello.
Tomemos en cuenta seriamente para aplicar a nuestro "tira y afloja" el derretimiento espontáneo en nuestros laboratorios del sistema físico en agua y sus hielos derritiéndose naturalmente a una benigna temperatura termal de 20 °C. Evaluando esto determinamos que ocurre con certeza lo impensado. Sabemos de hecho por sentido común termodinámico que el agua aquí requiere forzosamente absorber y tomar calor, lo cual a nivel físico significa explícitamente estar dispuesto a «perder» un lado del tira y afloja y ser derrotado en este terreno.
¿Qué sucede analíticamente al contrastarlo? Que paralelamente, todas las formaciones moleculares logradas pasadas a la fase de flujo acuático del , a su vez, quedan por una diferencia abismal muy ampliamente más sueltas caóticamente a nivel de su distribución respecto a su antigua forma compacta, polar rígida e inútilmente unificada del formato como hielo sólido polar . Ese aumento asombroso en dicho rubro marca la diferencia: es finalmente que la tremenda y sublime ganancia masiva en dicho desorden molecular resulta tan exageradamente grande en todos los horizontes posibles que en suma compensa de sobra por entero al mismo y exigente requerimiento abrumador de su respectiva energía calórica base endotérmica subyacente de su contraparte.
Así a gran magnitud se concluye todo; una vez compensado, la espléndida naturaleza decide inequívoca y triunfalmente que como es lógico, el desorden general gana la contienda. Derivado de todo lo abarcado, el proceso biológico o termodinámico en disyuntiva corre triunfante y ocurre final y definitivamente, en todos sus ámbitos, espontáneamente. Donde la temperatura en turno de la sala biológica actúa en sí misma como el factor más definitorio que modula y regula tal maravilla incesante; controlando así la balanza de fuerzas para acercarse en una armonía total a nuestro equilibrio químico.
Resumen de Espontaneidad (ΔG = ΔH - TΔS)
| Término de Entalpía (ΔH) | Término de Entropía (ΔS) | Energía Libre (ΔG) | ¿Cuándo es espontánea? |
|---|---|---|---|
| Negativa (<
0) Libera calor |
Positiva (>
0) Aumenta desorden |
Siempre (-) | Siempre espontánea a cualquier temperatura. |
| Positiva (> 0) Absorbe calor |
Negativa (< 0) Disminuye desorden |
Siempre (+) | Nunca espontánea (el proceso inverso sí lo es). |
| Negativa (<
0) Libera calor |
Negativa (< 0) Disminuye desorden |
Depende (-) o (+) | Espontánea solo a Bajas Temperaturas. |
| Positiva (> 0) Absorbe calor |
Positiva (>
0) Aumenta desorden |
Depende (-) o (+) | Espontánea solo a Altas Temperaturas. |

Podcast: Introducción al Equilibrio Químico
Escucha una narración explicativa sobre cinética, espontaneidad, energía libre y equilibrio químico.
Video Educativo: Introducción al Equilibrio Químico
Presentación en PDF: Cinética y Termodinámica hacia el Equilibrio
Para mejor experiencia en celular, abre la presentación directamente:
Abrir Presentación PDFVisualiza la presentación.
Infografía: Introducción al Equilibrio Químico

- 1. ¿Cuál es la diferencia esencial entre cinética y termodinámica?
- 2. ¿Por qué el diamante puede ser termodinámicamente inestable y aun así persistir?
- 3. ¿Qué representa la situación B de la piedra en la colina?
- 4. ¿Qué indica el signo negativo de ΔG?
- 5. ¿Por qué el sulfato de bario puede utilizarse en radiología si el bario iónico es tóxico?
- 6. ¿Qué significa que el equilibrio químico sea dinámico?
- 7. ¿Cuál es la diferencia entre un proceso exergónico y uno exotérmico?
- 8. ¿Por qué la temperatura puede modificar la espontaneidad de un proceso?
- 9. ¿Qué caracteriza a la situación C en términos energéticos?
- 10. ¿Por qué el derretimiento del hielo a 20 °C ayuda a entender el papel de la entropía?
-
Explique por qué un proceso puede ser espontáneo desde el punto de vista termodinámico
y, sin embargo, avanzar muy lentamente desde el punto de vista cinético.
-
Analice la analogía de la piedra en la colina y relacione cada situación con
espontaneidad, energía de activación y signo de ΔG.
-
Explique cómo el caso clínico del sulfato de bario ilustra la importancia del
equilibrio químico en medicina.
-
Utilice la ecuación ΔG = ΔH - TΔS para explicar por qué algunos procesos son
espontáneos solo a altas temperaturas y otros solo a bajas temperaturas.
-
Compare cuidadosamente las parejas exergónico/endergónico y exotérmico/endotérmico, e
indique por qué no deben usarse como sinónimos.
-
Analice por qué el equilibrio químico no debe interpretarse como “ausencia de cambio”
y discuta las consecuencias de esta idea errónea en la enseñanza de la química.
-
Para un proceso químico se tiene ΔH = -45 kJmol y ΔS = -120 Jmol·K. Determine si el
proceso es espontáneo a 25 °C.
-
Un proceso presenta ΔH = +32 kJmol y ΔS = +95 Jmol·K. Calcule la
temperatura mínima a partir de la cual el proceso se vuelve espontáneo.
-
Evalúe el signo de ΔG a 298 K para un cambio con ΔH = +18 kJmol y ΔS = -60 Jmol·K. Indique si es
espontáneo o no.
-
Una reacción tiene ΔH = -12 kJmol y ΔS = +40 Jmol·K. Calcule ΔG a 300 K y
clasifique el proceso.
-
Si una reacción tiene ΔH = -80 kJmol y ΔS = -220 Jmol·K, compare su
espontaneidad a 250 K y a 500 K.
-
En una reacción, ΔG = -15 kJmol pero la energía de
activación es muy alta. ¿Qué puede concluirse sobre su espontaneidad y sobre su
rapidez?