Instrucciones
Cargar archivo PDB
Diferentes formas de representación de las moléculas
- "Amino" es un esquema que asigna colores a los aminoácidos en función de sus propiedades químicas, p. ácido, básico, hidrofóbico o polar. Los colores son ASP, GLU, CYS, MET, LYS, ARG, SER, THR, PHE, TYR, ASN, GLN, GLY, LEU, VAL, ILE, ALA, TRP, HIS y PRO. Los ácidos nucleicos son de color caré claro en el esquema "amino".
- "Cadena" es un esquema que da un color diferente a cada cadena del archivo pdb.
- "Grupo" es un esquema que colorea las cadenas de proteínas de manera diferencial en la dirección amino-carboxi. Este esquema también colorea las cadenas de ácido nucleico de manera diferencial en la dirección 5 '> 3'.
- "Temperatura" es un esquema que colorea los átomos de acuerdo con sus temperaturas anisotrópicas, almacenadas como un valor beta en un archivo pdb. La temperatura anisotrópica indica la movilidad de un átomo o la incertidumbre de posición. Los segmentos más "móviles" y más cálidos son de color rojo, progresando a fragmentos azules más inmóviles.
- "Estructura" es un esquema de color muy útil porque colorea de manera diferencial la estructura secundaria de una proteína (hélices α y láminas β). Es mejor usar un comando de visualización que ilustre la estructura secundaria cuando se utiliza el esquema de colores de la estructura (por ejemplo, cintas, dibujos animados, esqueleto, trazas o hebras; consulte la sección Visualización).
Clasificación de los aminoácidos
- Ácidos: Asp, Glu
- No cíclicos
- Alifáticos: Ala, Gly, Ile, Leu, Val
- Aromáticos: His, Phe, Trp, Tyr
- Básicos: Arg, His, Lys
- Interiores: Ala, Leu, Val, Ile, Phe, Cys, Met, Trp
- Con carga: Asp, Glu, Arg, His, Lys
- Hidrofóbicos: Ala, Leu, Val, Ile, Pro, Phe, Met, Trp
- Polares: Cys, Gly, Ser, Thr, Lys, Asp, Asn, Glu, Arg, Gln, Tyr, His
- Pequeños: Ala, Gly, Ser
Metales
Grupos Prostéticos
Superficie y Cavidades
Sección
Laboratorio de IA: Tu Copiloto de Estudio
Aprende a usar la Inteligencia Artificial Científica
La IA puede ayudarte a razonar con mayor profundidad la cinética química si la usas con preguntas bien planteadas. Aquí tienes 6 prompts listos para analizar velocidad de reacción, energía de activación, choques efectivos y catálisis.
1. Teoría de las Colisiones
Choques efectivos y orientación molecular.
2. Energía de Activación
Barrera energética y estado activado.
3. Ley de Velocidad
Concentración y orden de reacción.
4. Temperatura y Arrhenius
Energía cinética y rapidez de reacción.
5. Inhibición Enzimática Clínica
Farmacología, sitio activo y velocidad de reacción.
6. Catalizadores y Enzimas
Disminución de la Ea y selectividad biológica.
Equilibrio Químico
La cinética química es el estudio de las velocidades de las reacciones químicas y de los factores que influyen en ellas. La velocidad de reacción es una medida de la rapidez con que se forman los productos a partir de los reactantes. Algunas reacciones ocurren casi instantáneamente. En estas reacciones, con sólo ponerse en contacto los reactantes se transforman totalmente en productos. Las explosiones son ejemplos de reacciones inmediatas. Otras reacciones tienen velocidades tan lentas que pueden pasar años antes de que la reacción se complete. La mayoría de las reacciones químicas suceden a velocidades intermedias entre estos dos extremos.
Las velocidades de las reacciones químicas se miden, por la determinación de la disminución de la concentración de los reactantes, o del aumento de concentración de los productos, en un intervalo de tiempo específico.
En una reacción con una velocidad de reacción alta, el intervalo de tiempo para que ocurra dicha reacción es relativamente corto. Una reacción que se efectúa a velocidades menores, requiere más tiempo para realizarse.
¿Cómo se expresa la velocidad de reacción?
La velocidad de reacción puede expresarse de manera cuantitativa como el cambio de concentración de reactivos o productos por unidad de tiempo. En lenguaje experimental, esto significa medir cuánto disminuye una especie reactiva o cuánto aumenta una especie producto mientras transcurre el proceso químico.
Expresión general de velocidad
Para una reacción del tipo:
la velocidad puede escribirse como:
Los factores 1/a, 1/b, 1/c y 1/d indican que el cambio de concentración de cada especie debe dividirse entre su coeficiente estequiométrico. Esto se hace porque reactivos y productos no siempre se consumen o se forman en la misma proporción numérica.
En otras palabras, las letras a, b, c y d corresponden a los coeficientes de la ecuación química ajustada. Al dividir por ellos, todas las expresiones representan una sola velocidad de reacción común. Por ejemplo, si una especie tiene coeficiente 2, su concentración puede cambiar el doble de rápido que otra con coeficiente 1; dividir entre ese 2 corrige la comparación.
El signo negativo se utiliza para los reactivos porque su concentración disminuye; el signo positivo se usa para los productos porque su concentración aumenta.
Velocidad media y velocidad instantánea
La velocidad media se calcula a lo largo de un intervalo finito de tiempo y es útil cuando se comparan resultados experimentales entre dos mediciones. En cambio, la velocidad instantánea describe lo que ocurre en un instante particular y corresponde, gráficamente, a la pendiente de la curva concentración-tiempo en ese punto.
En las primeras etapas de una reacción, la velocidad suele ser mayor porque la concentración de los reactivos es más alta y la probabilidad de colisiones efectivas también aumenta. Conforme los reactivos se consumen, las colisiones útiles se vuelven menos frecuentes y la rapidez disminuye, salvo que exista un cambio externo como temperatura, presión o catalizadores.
Lectura del simulador de velocidad y equilibrio
En esta página dispones de un simulador interactivo que funciona como una pequeña experiencia de laboratorio computacional. Su propósito es que puedas manipular condiciones iniciales, observar gráficas en tiempo real y analizar cómo el sistema evoluciona hasta alcanzar el equilibrio dinámico.
El simulador de esta página permite observar tres ideas fundamentales:
- La concentración de N2O4 disminuye cuando predomina la reacción directa y la de NO2 aumenta.
- La velocidad directa y la velocidad inversa cambian continuamente, pero el equilibrio dinámico se alcanza cuando ambas se igualan.
- La comparación entre Qc y Kc permite predecir hacia qué lado evoluciona el sistema antes de llegar al equilibrio.
De esta manera, el estudiante no solo lee la teoría, sino que también experimenta virtualmente con un modelo cinético y comprueba cómo las ecuaciones se reflejan en el comportamiento del sistema químico.
Velocidad de reacción y equilibrio dinámico
En una reacción reversible, la velocidad no debe interpretarse solo como un proceso que avanza hacia los productos. A medida que se forman productos, estos también pueden reaccionar entre sí para regenerar reactivos. Por ello, en muchos sistemas existe una velocidad directa y una velocidad inversa. Al inicio, la reacción directa suele ser dominante; sin embargo, conforme aparecen productos, la reacción inversa empieza a adquirir importancia hasta que ambas velocidades se igualan.
Cuando se alcanza este punto, el sistema entra en equilibrio dinámico: las concentraciones macroscópicas permanecen constantes, aunque a nivel microscópico las moléculas siguen chocando y reaccionando en ambos sentidos. Este concepto es esencial porque conecta la cinética química con el equilibrio químico y ayuda a comprender por qué un sistema puede parecer estático aunque internamente continúe activo.
Desglose matemático: obtención de Keq al igualar velocidades
Para la reacción reversible del simulador:
las expresiones cinéticas son:
En el equilibrio dinámico se cumple que ambas velocidades son iguales:
Ahora despejamos el cociente de concentraciones de equilibrio:
Esto significa que, para este sistema, la constante de equilibrio puede interpretarse como la razón entre la constante de velocidad de la reacción directa y la constante de velocidad de la reacción inversa.
¿Qué modifica el valor de Keq?
La temperatura sí modifica el valor de Keq porque altera de manera diferente las constantes cinéticas de la reacción directa e inversa. Como en este tema se ha mostrado que:
Keq = kd / ki
si la temperatura cambia, normalmente cambian kd y ki, y por tanto también cambia el valor de Keq.
La diferencia entre variables que sí cambian Keq y variables que no lo cambian a temperatura constante puede resumirse así:
| Variable | ¿Modifica Keq? | Efecto principal |
|---|---|---|
| Temperatura | Sí | Cambia kd y ki; por eso cambia el valor de Keq. |
| Concentración inicial | No | Modifica Q y desplaza temporalmente el sistema, pero no altera Keq. |
| Presión o volumen | No | En sistemas gaseosos puede desplazar la posición del equilibrio, pero Keq permanece igual si la temperatura no cambia. |
| Catalizador | No | Acelera por igual la reacción directa e inversa; solo permite alcanzar el equilibrio más rápido. |
| Superficie de contacto o agitación | No | Puede afectar la velocidad observada del proceso, pero no el valor termodinámico de Keq. |
Aplicaciones médicas de la velocidad de reacción
La cinética química tiene aplicaciones directas en medicina porque permite comprender y controlar la rapidez con la que ocurren procesos biológicos y terapéuticos.
- Hematosis alveolar: el intercambio de O2 y CO2 en los pulmones depende de la rapidez de difusión y de colisión de las moléculas.
- Hemodiálisis: la transferencia de sustancias a través de membranas se basa en gradientes de concentración y velocidades de transporte molecular.
- Absorción de medicamentos: la superficie de contacto influye en la rapidez con que un fármaco se disuelve, se absorbe y empieza a producir efecto.
- Farmacocinética: la concentración inicial de un medicamento afecta la velocidad de su metabolismo y eliminación en el organismo.
- Control térmico clínico: la fiebre acelera reacciones metabólicas, mientras que la hipotermia inducida puede disminuirlas para proteger tejidos.
- Inhibición enzimática: muchos fármacos, como algunos antiinflamatorios, actúan reduciendo o bloqueando la velocidad de reacciones catalizadas por enzimas.
Simulador: Variación de las concentraciones con el tiempo
Factores de Reacción
Ajusta los factores para observar en tiempo real la concentración de N2O4 (rojo) y la concentración de NO2 (azul).
Teoría Cinético Molecular
La teoría cinética de los gases explica las características y propiedades de la materia en general, y establece que el calor y el movimiento están relacionados, que las partículas de toda materia están en movimiento hasta cierto punto y que el calor es una señal de este movimiento.
Las velocidades de las reacciones químicas se explican teóricamente por la teoría de las colisiones. La premisa básica de la teoría de las colisiones es que para que dos sustancias reaccionen, las partículas deben chocar entre sí. Después del choque, existen dos posibilidades: se rompen los enlaces en las moléculas de los reactantes y se forman los enlaces en los productos, la colisión se llama colisión efectiva (sólo se observa una colisión efectiva), y si la colisión no genera productos, la colisión se denomina colisión inefectiva.
En el cuerpo humano, comprender cómo el movimiento molecular aleatorio rige la frecuencia de las colisiones es vital para entender no solo las biotransformaciones químicas (metabolismo), sino también la transferencia y difusión de sustancias vitales. Por ejemplo, el movimiento cinético rige los gradientes de concentración a través de las membranas celulares, dictando procesos clínicos primordiales como la hematosis alveolar (el intercambio de oxígeno y dióxido de carbono en los pulmones) y consolida los principios físico-químicos que permiten el intercambio extra-corpóreo en una máquina de hemodiálisis para pacientes renales.
Exploración sugerida con laboratorio computacional
En lugar de un video pasivo, esta sección se apoya ahora en los simuladores interactivos de la página para que el estudiante observe el fenómeno como si estuviera en un laboratorio computacional.
Para comprender la velocidad de reacción, conviene abrir el simulador de velocidad y equilibrio y analizar cómo cambian las concentraciones de N2O4 y NO2 con el tiempo. Para estudiar la barrera energética, la ruptura del enlace N-N y la formación de productos, se recomienda usar el botón Simulación 3: Laboratorio Virtual de Cinética de Reacciones, que acabamos de incorporar a esta página.
- Observa cuándo la velocidad directa y la inversa llegan a ser iguales.
- Compara el comportamiento del sistema cuando cambias las concentraciones iniciales.
- Relaciona la barrera de energía de activación con la formación o no de productos usando el botón Simulación 3: Laboratorio Virtual de Cinética de Reacciones.
Para que ocurra un choque efectivo y, por ende, una reacción química, se deben cumplir dos requisitos fundamentales de la Teoría de las Colisiones:
- Energía de activación: En la reacción N2O4 → 2 NO2, una molécula de N2O4 debe recibir, mediante choques con otras moléculas del sistema, energía suficiente para debilitar y romper el enlace N-N, superando así la barrera energética.
- Transferencia eficaz de energía: No todo choque entre moléculas de N2O4 produce reacción. Para que el choque sea efectivo, una fracción suficiente de la energía transferida debe canalizarse hacia el enlace N-N de una de las moléculas, favoreciendo su separación en dos fragmentos NO2.
Choque interactivo sobre N2O4
Ajusta la energía del choque entre dos moléculas de N2O4 y la fracción de esa energía que se transfiere al enlace N-N de la molécula objetivo. Si ambas condiciones son suficientes, el enlace se rompe y se forman 2 NO2; si no, el choque es inefectivo.
Criterio didáctico del modelo: el choque se considera efectivo cuando la energía total del choque es al menos 60% y la fracción transferida al enlace N-N es al menos 55%.
Energía de Activación
La energía de activación es la energía mínima necesaria para que tenga lugar una reacción. En el simulador de esta página, esa energía corresponde a la cantidad mínima que necesita la molécula de N2O4 para atravesar el máximo de la curva de energía potencial y transformarse en 2 NO2.
Si la energía suministrada es menor que la energía de activación, la molécula no logra romper el enlace N-N y permanece como reactivo. En cambio, cuando la energía es igual o mayor que esa barrera, ocurre una activación efectiva y se observa la formación de los productos, tal como se representa en el laboratorio virtual.
Perfil energético interactivo
Esta versión compara de forma simultánea una reacción exotérmica y una endotérmica con una representación más sencilla. Puedes variar una barrera de activación moderada y la magnitud de ΔH para observar cómo cambia la altura del máximo energético y la posición de los productos.
Esta representación es comparativa y no pretende fijar una relación universal entre Ea y |ΔH|. Se usa una escala pedagógica para evitar confundir la barrera de activación con el cambio global de entalpía.
Factores que afectan la velocidad de reacción
Teniendo en cuenta los planteamientos de la teoría de las colisiones, cualquier condición que afecte la ocurrencia de choques efectivos, afectará igualmente la velocidad de reacción. Experimentalmente se ha establecido que los principales factores determinantes de la velocidad de las reacciones químicas son: la naturaleza y concentración de los reactivos, la temperatura a la que ocurre la reacción y la presencia de catalizadores.
Panel integrador de factores
Ajusta estos cuatro factores de forma didáctica. El indicador final no representa una ley universal exacta, pero sí resume cómo aumenta o disminuye la probabilidad de choques efectivos.
Naturaleza de los reactivos
La tendencia a reaccionar que muestran unas sustancias con otras se relaciona con la distribución y estructura tridimensional de los electrones periféricos, con la energía de los enlaces que unen los diferentes átomos y con la afinidad entre átomos, moléculas o iones presentes. Por ejemplo, las sustancias en formas moleculares reaccionan más lentamente que las iónicas.
Comparador interactivo de naturaleza química
Selecciona distintos tipos de reactivos para comparar afinidad, barrera de ruptura/reorganización y velocidad relativa esperada.
Video Educativo: Reactividad de litio, sodio y potasio
Superficie de contacto
Mientras más puntos de contacto haya entre las sustancias reaccionantes, la reacción ocurrirá más rápido. Por ejemplo, un terrón de azúcar es atacado por bacterias y levaduras, más lentamente que si se hallara disuelto en una solución acuosa. En el ámbito de la farmacología, la superficie de contacto determina cómo actúan los medicamentos según sus vías de administración: una pastilla sólida requiere disgregarse y disolverse antes de absorberse de forma celular, mientras que un medicamento administrado como polvo liofilizado, solución o emulsión tiene una superficie de contacto maximizada, logrando una absorción sistémica y un efecto terapéutico mucho más rápido.
Superficie de contacto y velocidad
Compara una tableta entera, fragmentada o pulverizada. A mayor área expuesta al solvente, más puntos de ataque y mayor rapidez observable.
Interpretación del esquema: la figura blanca representa una tableta efervescente; sus fragmentos muestran el sólido antes de disolverse. Los puntos azules móviles representan moléculas del medio reactivo/solvente que chocan con la superficie, y los círculos traslúcidos ascendentes representan la efervescencia o liberación de gas durante la reacción.

Video Educativo: Superficie de contacto en Alka Seltzer
Concentración de los reactivos
A partir de la ecuación de velocidad sabemos que la velocidad es proporcional a la concentración de las especies químicas. Esto se debe a que al aumentar la concentración de las sustancias reaccionantes, se aumenta la probabilidad de choque entre sus moléculas, y por tanto la cantidad de colisiones efectivas. Por ejemplo, una granalla de zinc reacciona más rápidamente con ácido clorhídrico 12 molar que con ácido clorhídrico 6 molar. Cuando reacciona con ácido nítrico 6 molar ocurre una reacción de simple desplazamiento, pero cuando reacciona con ácido nítrico 15 molar, la concentración es tan elevada que favorece una reacción de oxidación redox. Conceptualmente, esto se aplica directamente a la biodisponibilidad y farmacocinética clínica de los medicamentos: a mayor concentración inicial de un fármaco en el plasma sanguíneo, la tasa a la cual el hígado comienza a metabolizarlo y el organismo a eliminarlo es inicialmente mayor (cinética de primer orden).

Video Educativo: Efecto de la concentración
Cuando los reactivos son gases, un aumento en la presión del sistema, genera un aumento del número de moléculas por unidad de área, lo que se traduce en un aumento de la concentración que lleva a su vez a una aceleración del proceso.
La magnitud en la cual se aumenta la velocidad, con cada aumento de concentración depende de la reacción y se debe determinar empíricamente.
Ley de velocidad y orden de reacción
Decir que la velocidad depende de la concentración no significa que siempre cambie en la misma proporción que la ecuación química ajustada. Experimentalmente, la rapidez suele expresarse mediante una ley de velocidad del tipo:
En esta expresión, k es la constante de velocidad, mientras que m y n son los órdenes parciales de reacción respecto de A y B. La suma m + n corresponde al orden global.
Estos exponentes no se toman automáticamente de los coeficientes estequiométricos de la ecuación global, salvo en mecanismos muy simples. Por eso el orden de reacción se obtiene a partir de datos experimentales.
Ejemplo: si al duplicar la concentración de A la velocidad se vuelve cuatro veces mayor, entonces:
En ese caso, la reacción es de segundo orden respecto de A. Si al duplicar la concentración la velocidad solo se duplicara, sería de primer orden; y si la velocidad no cambiara, sería de orden cero respecto de ese reactivo.
Concentración y frecuencia de choques
Mueve el control para aumentar el número de partículas en el mismo volumen. Observa cómo suben los choques totales y la fracción de choques efectivos.
Temperatura
Con base en la teoría de colisiones, así como en la teoría cinético-molecular, se comprende fácilmente que un aumento en la temperatura del sistema en reacción lleve a un aumento proporcional en la velocidad de reacción. A mayor temperatura, mayor energía cinética poseerán las moléculas y por tanto más cerca estarán de alcanzar el valor crítico, Ea. Así mismo, a mayor energía cinética, la frecuencia de choques se verá también incrementada, y por tanto, la probabilidad de choques efectivos aumentará. Este principio químico explica por qué fenómenos como la fiebre (aumento de la temperatura corporal) aceleran el metabolismo basal y la respuesta de síntesis inmunológica. Por el contrario, en procedimientos quirúrgicos donde hay bajo flujo sanguíneo (ej. corazón abierto), los médicos utilizan la hipotermia inducida de forma terapéutica para ralentizar las reacciones químicas de degradación celular, protegiendo a los tejidos frente a una posible falta de oxígeno (isquemia).
Temperatura y fracción que supera Ea
La energía de activación se mantiene fija. Al elevar la temperatura, aumenta la fracción de moléculas con energía suficiente para superar la barrera.

La Alka Seltzer reacciona más rápidamente con agua caliente, luego con agua al tiempo y por último con agua fría.
Video Educativo: Efecto de la temperatura
Catalizadores
Un catalizador es una sustancia que afecta la velocidad de una reacción, ya sea incrementándola o retardándola. Los catalizadores se caracterizan porque son necesarios en muy bajas concentraciones y porque no son consumidos o transformados al final de la reacción. En ocasiones un catalizador puede intervenir en la reacción formando compuestos intermedios, que sirven de puente para la formación de los productos, pero al finalizar la reacción, la sustancia catalizadora siempre queda libre e inalterada.
El proceso general de alteración de la velocidad a través del empleo de catalizadores, recibe el nombre de catálisis. Cuando una sustancia actúa acelerando la reacción general se denomina catalizador positivo, mientras que si la retarda se denomina catalizador negativo o inhibidor. Por ejemplo, el oxígeno se puede obtener en el laboratorio por descomposición térmica del clorato potásico (KClO3), a 500 °C. Sin embargo, si se adiciona una pequeña cantidad de dióxido de manganeso, MnO2, la reacción ocurre a 150 °C, según la ecuación:
La acción de un catalizador se puede sintetizar como la disminución del valor crítico de energía, Ea, necesario para que la reacción ocurra. Los mecanismos para lograr esta disminución varían, desde la adsorción y por tanto, retención de los reactivos, hasta la formación de complejos activados entre reactivos y catalizadores. Es fundamental diferenciar rigurosamente entre verdaderos catalizadores formales (que disminuyen la energía de activación sin consumirse) y simples sustancias auxiliares como medios iónicos (por ejemplo, usar sal común para mejorar la conductividad en una cubeta de laboratorio), los cuales actúan favoreciendo medios pero no reducen la Ea propiamente dicha.
Comparador catalizado vs no catalizado
Activa la ruta catalizada o modifica la disminución de la barrera. Observa que el catalizador cambia la altura de Ea, pero no la energía inicial de reactivos ni la energía final de productos.
Catalizadores Biológicos
En los organismos vivos ocurren un sinnúmero de reacciones químicas, muchas de las cuales requerirían temperaturas o concentraciones demasiado altas para ser posibles. La manera como se logra que se lleven a término a temperatura ambiente y con concentraciones bajas es por medio de los llamados catalizadores biológicos o enzimas. Actualmente, la aplicación de la acción enzimática de múltiples sustancias orgánicas en la industria de alimentos, se halla muy desarrollada.
Video Educativo: Catálisis enzimática
La es una enzima que puede realizar proteólisis. La quimotripsina consiste en una cadena polipeptídica de 245 residuos, con cinco enlaces disulfuro (-S-S-). Es una enzima digestiva encargada de degradar las proteínas de los alimentos en el intestino, Ver con los aminoácidos responsables de la actividad catalítica en colores.
Escojemos este ejemplo de la quimotripsina, porque aunque es de un nivel de profundidad superior teóricamente, ilustra como se pueden llevar a cabo las reacciones a nivel del organismo. Electrónicamente son muchos procesos los que se llevan a cabo, pero lo maravilloso en nuestro organismo, es que son muy rápidos y muy específicos.
Así como las enzimas aceleran procesos vitales, también es posible ralentizarlos o bloquearlos en la práctica clínica empleando inhibidores enzimáticos. Gran parte de la terapéutica médica actual se basa en este importante principio; por ejemplo, el uso de medicamentos Antiinflamatorios No Esteroideos (AINEs, como la aspirina o ibuprofeno) se encarga de inhibir con precisión la enzima ciclooxigenasa (COX). Al bloquear su tríada u orificio activo, se impide que la enzima produzca prostaglandinas mediadoras del dolor, disminuyendo en consecuencia la reacción inflamatoria celular del paciente.

Podcast: Introducción a la Cinética Química
Escucha una explicación introductoria sobre velocidad de reacción, factores cinéticos y energía de activación.
Video Explicativo: Velocidad de Reacción
Presentación: Velocidad de Reacción
Para mejor experiencia en celular, abre la presentación directamente:
Abrir Presentación PDFVisualiza la presentación de velocidad de reacción.
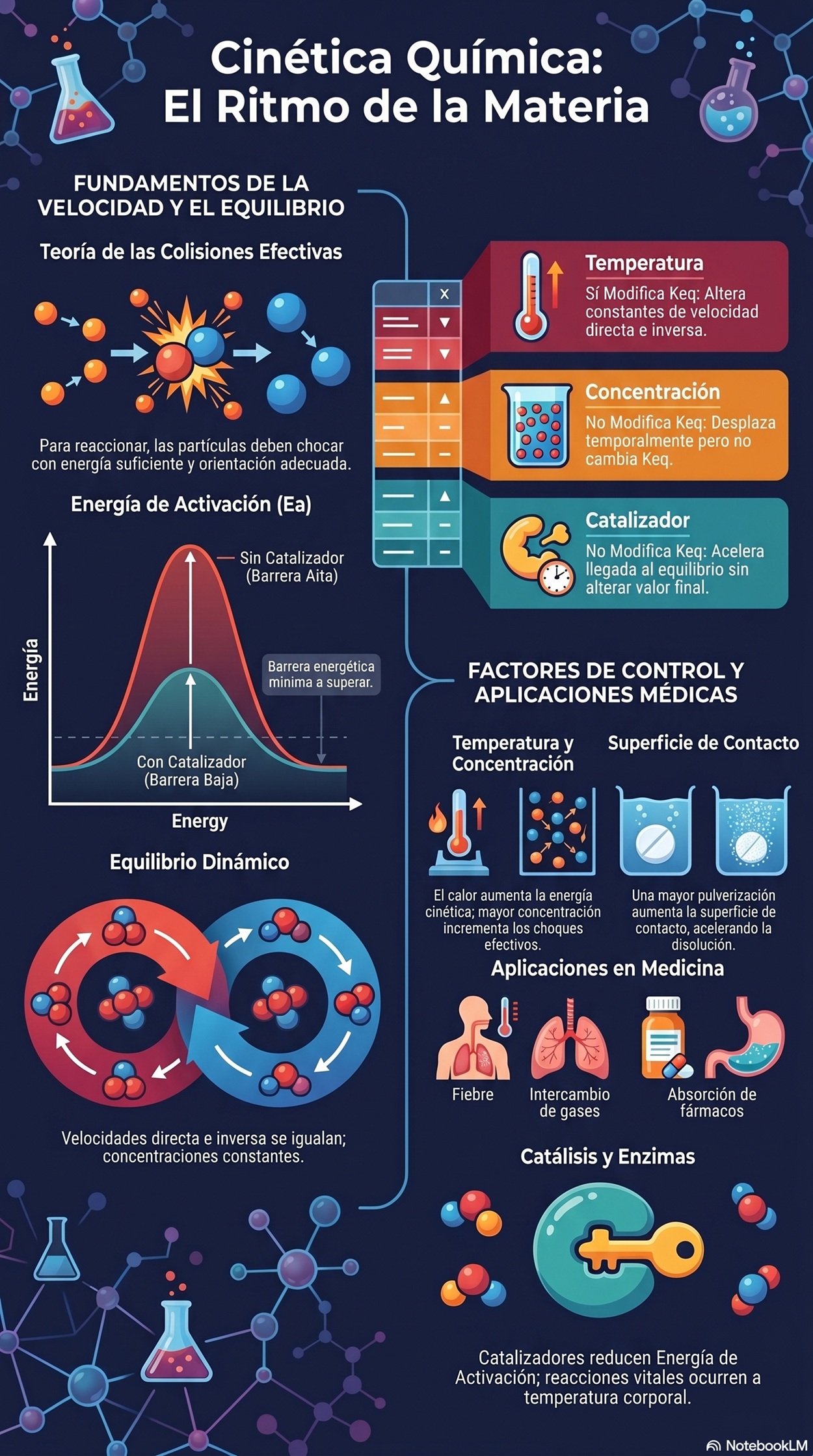
Infografía: Velocidad de Reacción
Resume de forma visual los conceptos clave de cinética química: definición de velocidad, factores que la modifican y relación con el equilibrio.
- 1. ¿Qué estudia la cinética química?
-
La cinética química estudia la rapidez con la que ocurren las reacciones, los factores que modifican esa rapidez y el mecanismo por el cual los reactivos se transforman en productos.
- 2. ¿Por qué no toda colisión entre partículas produce reacción?
-
Porque para que un choque sea efectivo las partículas deben tener energía suficiente para superar la energía de activación y, además, una orientación adecuada para reorganizar enlaces.
- 3. ¿Qué representa la energía de activación (Ea)?
-
Representa la barrera energética mínima que deben vencer los reactivos para alcanzar el estado activado y poder convertirse en productos.
- 4. ¿Cómo afecta un aumento de concentración a la velocidad de reacción?
-
En general, al aumentar la concentración se incrementa el número de partículas por unidad de volumen, lo que hace más frecuentes los choques y tiende a aumentar la velocidad de reacción.
- 5. ¿Por qué el aumento de temperatura acelera la reacción?
-
Porque aumenta la energía cinética media de las moléculas y, por tanto, la fracción de partículas que puede superar la energía de activación durante una colisión.
- 6. ¿Por qué un sólido pulverizado suele reaccionar más rápido que un bloque entero?
-
Porque al pulverizarlo aumenta la superficie de contacto, dejando expuestas más partículas reactivas al medio y favoreciendo más choques por intervalo de tiempo.
- 7. ¿Qué efecto tiene un catalizador sobre la energía de activación?
-
Un catalizador proporciona una ruta alternativa de reacción con menor Ea, de modo que una fracción mayor de colisiones puede producir reacción.
- 8. ¿Un catalizador modifica el valor de Keq?
-
No. El catalizador no cambia la posición del equilibrio ni el valor de Keq; solo permite alcanzar el equilibrio más rápidamente.
- 9. ¿Cuál es la diferencia entre velocidad de reacción y espontaneidad?
-
La velocidad indica qué tan rápido ocurre un proceso, mientras que la espontaneidad indica si el proceso es favorable termodinámicamente. Una reacción puede ser espontánea y, aun así, ser lenta.
- 10. Mencione una aplicación médica de la cinética química.
-
Un ejemplo es la inhibición enzimática por fármacos, donde se disminuye la velocidad de reacciones biológicas específicas para lograr un efecto terapéutico, como ocurre con varios antiinflamatorios o estatinas.
-
Explique por qué la teoría de las colisiones no se limita a decir que “si chocan,
reaccionan”.
Debe integrarse el papel de la energía mínima, la orientación molecular y la formación del complejo activado. No basta con mencionar frecuencia de choque. -
Analice cómo concentración, temperatura y superficie de contacto modifican la
velocidad de reacción por mecanismos distintos.
La respuesta debe distinguir entre frecuencia de encuentro, energía cinética media y área expuesta. No son factores equivalentes aunque todos aumenten la rapidez observada. -
Desarrolle la diferencia entre catalizador, inhibidor y sustancia auxiliar del medio
de reacción.
Debe aclararse que un catalizador modifica la ruta y disminuye Ea, mientras que un inhibidor reduce la velocidad. Una sustancia auxiliar puede favorecer condiciones del sistema sin actuar como catalizador verdadero. -
Explique por qué una reacción puede ser muy rápida pero no cambiar Keq.
Debe destacarse que la cinética gobierna la rapidez y la termodinámica gobierna la posición del equilibrio. Un catalizador acelera la llegada al equilibrio, pero no altera su valor termodinámico. -
Relacione la cinética química con un problema clínico real.
Puede abordarse con ejemplos como fiebre e hipotermia, absorción de medicamentos, inhibición enzimática o metabolismo de fármacos. Debe existir relación clara entre factor cinético y consecuencia biológica. -
Compare la catálisis química de MnO2 con la catálisis biológica de una
enzima.
Debe compararse la disminución de Ea, pero también la especificidad, el sitio activo y la relevancia fisiológica de las enzimas como catalizadores altamente selectivos.
-
Para una reacción se observa que al duplicar la concentración de A la velocidad pasa
de 0.20 a 0.80 mol/L·s, manteniendo constante todo lo demás. Determine el orden
respecto de A.
Si al duplicar [A] la velocidad se hace 4 veces mayor, entonces $2^n = 4$. Por tanto, n = 2. La reacción es de segundo orden respecto de A. -
En otra reacción, al triplicar la concentración de B la velocidad aumenta de 0.50 a
1.50 mol/L·s. Determine el orden respecto de B.
El factor de cambio es 3. Entonces $3^n = 3$, por lo que n = 1. La reacción es de primer orden respecto de B. -
La ley de velocidad es v = k[A]2[B]. Si [A] se duplica y [B] se mantiene
constante, ¿por cuánto cambia la velocidad?
Como A está al cuadrado, la velocidad cambia por $2^2 = 4$. La rapidez se vuelve cuatro veces mayor. -
La ley de velocidad es v = k[A][B]. Si [A] se reduce a la mitad y [B] se duplica,
¿cómo cambia la velocidad?
El factor total es $(1/2)(2) = 1$. Por tanto, la velocidad no cambia. -
Una reacción tiene constante de velocidad k = 0.030 s-1 a 25 °C y k = 0.060
s-1 a 35 °C. ¿En cuánto cambió k al aumentar la temperatura 10 °C?
La constante pasó de 0.030 a 0.060 s-1, por lo que se duplicó. El factor de cambio fue 2. -
Si una reacción sin catalizador requiere 72 kJ/mol para superar la barrera y un
catalizador reduce esa barrera a 46 kJ/mol, ¿en cuánto disminuyó la energía de
activación?
La disminución es $72 - 46 = 26$. La energía de activación bajó en 26 kJ/mol.