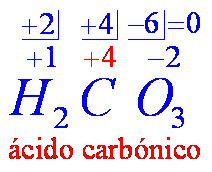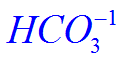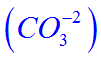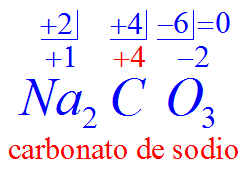Instrucciones
Usted tiene las siguientes opciones en este simulador para moléculas pequeñas tanto inorgánicas como orgánicas.
- En la parte superior, aparecen los botones 2D y 3D para que pueda observar el modelo en dos o tres dimensiones.
- A continuación se presenta el modelo en dos o tres dimensiones.
- "Search" puede ser utilizado para buscar alguna molécula, escribiendo el nombre en inglés, por ejemplo al escribir, sulphuric acid (ácido sulfúrico).
- Color de fondo, sirve seleccionar el color del fondo del modelo en tres dimensiones.
- Girar X, Y, Z, para girar el modelo en tres dimensiones en los ejes x, y, z.
- Alambres, varillas y pelotas y varillas, para cambiar el modelo en tres dimensiones en esas representaciones.
- Energía, aparce en la parte superior la energía de la molécula en kJ/mol o kcal/mol.
- Minmizar por MMFF94, normalmente las estructuras iniciales que se crean en los simuladores poseen energías mucho mayores a las que tendría un objeto real, por esta razón, se utilizan algoritmos para calcular las posiciones y fuerzas originales, con el objetivo de minimizarlas y que sean más realistas.
- Arrastrar Minimizar, usted puede arrastrar un átomo, soltarlo y entonces el sistema hace un cálculo de minimización de energía.
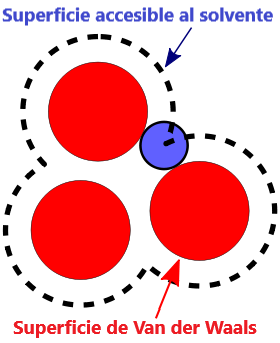
- Superficie VDW, La superficie de van der Waals de una molécula es una representación abstracta o modelo de esa molécula, que ilustra dónde, en términos muy generales, podría haber una superficie para la molécula en función de los cortes duros de los radios de van der Waals para átomos individuales, y representa una superficie a través de la cual la molécula podría concebirse interactuando con otras moléculas.
- PEM es el mapa de potencial electrostático.
- Cargas parciales, para ver el valor de la carga relativa positiva o negativa de cada átomo.
- Tetraedros, para el caso que exista alguna átomo tetraédrico.
- Dipolos enlaces, para ver el los dipolos de todos los enlaces.
- Dipolo molecular, para ver el momento dipolar resultante de toda la molécula.
- Botón 2D, cuando escoge el botón 2D, la aplicación tiene su propio menú y quedan inhabilitados todos los botones 3D.
Nomenclatura
- Los oxiácidos se forman cuando reacciona un anhídrido con agua.
- La nomenclatura más utilizada corresponde al “Sistema Clásico”.
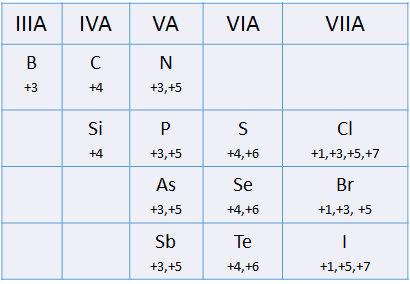
- En las fórmulas de abajo se indican los estados de oxidación especialmente el del elemento central (escrito con rojo), el que indica cual es el sufijo que se debe utilizar en su nombre.
Ejemplo:
y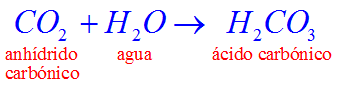
- En el ácido carbónico, el carbono tiene un estado de oxidación de +4. Sin embargo, a pesar de tener un estado de oxidación único, se le asigna el sufijo -ico. Esto debe considerarse como una excepción.
- El bicarbonato de sodio se deriva de la neutralización parcial del ácido carbónico y se puede nombrar de varias formas. También, se le considera como un compuesto cuaternario ya que esta formado de cuatro elementos diferentes.
- Cuando se nombra la sal se cambia el sufijo -ico por -ato.
- También se muestran otros bicarbonatos combinados con calcio y aluminio. En todos el átomo de carbono tiene un estado de oxidación de +4.
- Cuando se neutraliza completamente el ácido carbónico, pierde sus dos hidrógenos los cuales son remplazados por metales.