Instrucciones
Usted tiene las siguientes opciones en este simulador para moléculas pequeñas tanto inorgánicas como orgánicas.
- En la parte superior, aparecen los botones 2D y 3D para que pueda observar el modelo en dos o tres dimensiones.
- A continuación se presenta el modelo en dos o tres dimensiones.
- "Search" puede ser utilizado para buscar alguna molécula, escribiendo el nombre en inglés, por ejemplo al escribir, sulphuric acid (ácido sulfúrico).
- Color de fondo, sirve seleccionar el color del fondo del modelo en tres dimensiones.
- Girar X, Y, Z, para girar el modelo en tres dimensiones en los ejes x, y, z.
- Alambres, varillas y pelotas y varillas, para cambiar el modelo en tres dimensiones en esas representaciones.
- Energía, aparce en la parte superior la energía de la molécula en kJ/mol o kcal/mol.
- Minmizar por MMFF94, normalmente las estructuras iniciales que se crean en los simuladores poseen energías mucho mayores a las que tendría un objeto real, por esta razón, se utilizan algoritmos para calcular las posiciones y fuerzas originales, con el objetivo de minimizarlas y que sean más realistas.
- Arrastrar Minimizar, usted puede arrastrar un átomo, soltarlo y entonces el sistema hace un cálculo de minimización de energía.
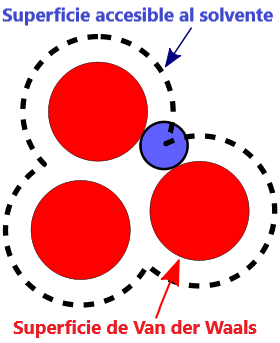
- Superficie VDW, La superficie de van der Waals de una molécula es una representación abstracta o modelo de esa molécula, que ilustra dónde, en términos muy generales, podría haber una superficie para la molécula en función de los cortes duros de los radios de van der Waals para átomos individuales, y representa una superficie a través de la cual la molécula podría concebirse interactuando con otras moléculas.
- PEM es el mapa de potencial electrostático.
- Cargas parciales, para ver el valor de la carga relativa positiva o negativa de cada átomo.
- Tetraedros, para el caso que exista alguna átomo tetraédrico.
- Dipolos enlaces, para ver el los dipolos de todos los enlaces.
- Dipolo molecular, para ver el momento dipolar resultante de toda la molécula.
- Botón 2D, cuando escoge el botón 2D, la aplicación tiene su propio menú y quedan inhabilitados todos los botones 3D.
Laboratorio de IA: Tu Copiloto de Estudio
Aprende a usar la Inteligencia Artificial Científica
La IA puede ayudarte a razonar con mayor profundidad el equilibrio químico y la cinética si la usas con preguntas bien planteadas. Aquí tienes 6 prompts listos para analizar velocidad de reacción, energía de activación, choques efectivos y catálisis.
1. Equilibrio Dinámico
Velocidades iguales y concentraciones constantes.
2. Constante de Equilibrio (Keq)
Significado y cálculo del cociente de reacción.
3. Le Châtelier: Concentración
Efecto de agregar o quitar sustancias.
4. Le Châtelier: Presión y Volumen
Comportamiento de sistemas gaseosos.
5. Le Châtelier: Temperatura
Reacciones exotérmicas y endotérmicas.
6. Aplicaciones Médicas del Equilibrio
Homeostasis y transporte de oxígeno.
Equilibrio Químico
Definición clave: El equilibrio químico es el estado dinámico en el que la velocidad de la reacción directa es igual a la velocidad de la reacción inversa; por ello, las concentraciones de reactivos y productos se mantienen constantes en el tiempo, aunque a nivel molecular las reacciones continúan ocurriendo en ambos sentidos.
El concepto de equilibrio es fundamental para conocer y entender la química y el comportamiento de las sustancias. En la constante de equilibrio se refleja la tendencia que tienen las sustancias de reaccionar, así como también, la dirección y magnitud del cambio químico. Todas las reacciones químicas pueden ser descritas bajo una condición de equilibrio.
Todos los sistemas químicos alcanzan en el tiempo la condición de equilibrio. El estado de equilibrio químico es de naturaleza dinámica y no estática.
Para comprender mejor esta idea, conviene observar cómo evolucionan las concentraciones de reactivos y productos a medida que transcurre el tiempo. En el siguiente simulador podrás modificar las cantidades iniciales de N2O4 y NO2 y ver de forma gráfica que, aunque al principio las concentraciones cambian rápidamente, llega un momento en el que ambas se estabilizan. Ese punto representa el equilibrio dinámico: las reacciones directa e inversa continúan ocurriendo, pero las concentraciones macroscópicas ya no varían de manera apreciable.
Simulador gráfico interactivo: N2O4 ⇌ 2NO2
Ingresa las concentraciones iniciales y observa cómo cambian con el tiempo hasta alcanzar el equilibrio dinámico. El punto verde marca el instante en el que las concentraciones dejan de cambiar de forma apreciable.
Ley de acción de masas (base para plantear Kc)
Antes de escribir la constante de equilibrio, se parte de la ley de acción de masas: la velocidad de una reacción es proporcional al producto de las concentraciones de las especies que reaccionan, cada una elevada a su coeficiente estequiométrico.
Para una reacción general aA + bB ⇋ cC + dD, se plantea:
vd = kd[A]a[B]b y vi = ki[C]c[D]d
Con esta base, al llegar al equilibrio se igualan ambas velocidades y se obtiene la expresión matemática de Kc.
Del simulador a la expresión matemática de Keq
En el simulador observaste que llega un instante en el que la velocidad directa y la velocidad inversa se igualan. Ese es el criterio cinético del equilibrio:
vd = vi
kd[Reactivos](coeficientes) = ki[Productos](coeficientes)
¿Por qué las velocidades se escriben así? Por la ley de acción de masas: la rapidez de cada sentido de reacción es proporcional al producto de las concentraciones de las especies que participan en ese sentido, y cada concentración se eleva a su coeficiente estequiométrico en la ecuación balanceada.
aA + bB ⇋ cC + dD
vd = kd[A]a[B]b y vi = ki[C]c[D]d
En equilibrio ambas velocidades se igualan; por eso aparece la relación kd[Reactivos](coeficientes) = ki[Productos](coeficientes).
Al reorganizar esta igualdad, se obtiene una constante que depende solo de la temperatura: la constante de equilibrio, Keq.
Para una ecuación balanceada general:
aA + bB ⇋ cC + dD
Keq (Kc) = [C]c[D]d[A]a[B]b
Significado de Kc: Kc es la constante de equilibrio expresada en términos de concentraciones molares (mol/L).
Es decir, en Keq se colocan las concentraciones de los productos en el numerador y las de los reactivos en el denominador, cada una elevada a su coeficiente estequiométrico.
Interpretación del desplazamiento del equilibrio
Después de una perturbación, el sistema puede desplazarse temporalmente hasta alcanzar de nuevo el equilibrio.
¿Qué es Qc? Qc es el cociente de reacción calculado con las concentraciones del instante analizado (no necesariamente en equilibrio):
Qc = [C]c[D]d[A]a[B]b
En otras palabras, Qc compara "cuánto producto hay" respecto a "cuánto reactivo hay" en ese momento. Luego se contrasta con Kc:
si Qc < Kc faltan productos y el sistema avanza hacia la derecha; si Qc > Kc sobran productos y el sistema se desplaza hacia la izquierda; si Qc = Kc, el sistema está en equilibrio.
La reacción sigue siendo reversible (⇋), pero durante el desplazamiento predomina temporalmente uno de los sentidos:
aA + bB ⇀↽ cC + dD
Desplazamiento hacia la derecha: predomina temporalmente el sentido directo (hacia productos).
Qc < Kc entonces vd > vi
aA + bB ⇀↽ cC + dD
Desplazamiento hacia la izquierda: predomina temporalmente el sentido inverso (hacia reactivos).
Qc > Kc entonces vi > vd
Cuando se restablece el equilibrio, ambas velocidades vuelven a igualarse: vd = vi y el símbolo vuelve a ser ⇋.
Ejemplo: N2(g) + 3H2(g) ⇌ 2NH3(g) (todos en fase gaseosa).
Equilibrio heterogéneo: Se da cuando los reactivos y/o productos están en diferentes fases (por ejemplo, sólidos y líquidos, o sólidos y gases).
Ejemplo: CaCO3(s) ⇌ CaO(s) + CO2(g) (sólidos y gas).
Principio de Le Chatelier y la energía libre en el simulador
El Principio de Le Chatelier establece que, si un sistema en equilibrio dinámico es sometido a una perturbación que cambie las condiciones (concentración, presión, volumen o temperatura), el sistema se desplazará en la dirección que tienda a contrarrestar dicha perturbación para alcanzar un nuevo estado de equilibrio.
Para comprender por qué ocurre esto desde una perspectiva termodinámica, nuestro simulador utiliza la analogía de un tubo en U. El nivel del fluido representa la Energía Libre de Gibbs (ΔG). Cuando los niveles están igualados, ΔG = 0 y el sistema está en equilibrio. Cualquier perturbación crea un desnivel (ΔG diferente de cero), y la reacción "fluirá" como un líquido cayendo cuesta abajo, hasta que los niveles se igualen nuevamente.
1. Efecto de los cambios en la Concentración
Teoría: Al agregar un reactivo o producto gaseoso o en solución, aumentamos su concentración. El sistema responderá consumiendo parte de la sustancia añadida. Matemáticamente, esto altera el Cociente de Reacción (Q), haciéndolo temporalmente mayor o menor que la constante Keq.
Compruébalo en el simulador:
- En la sección de Concentración, asegúrate de estar en modo Homogéneo N₂O₄ y haz clic en "+ Reactivo N₂O₄". Observarás que el nivel izquierdo sube (Q < Keq y ΔG < 0). El sistema reacciona espontáneamente hacia la derecha (productos). Presiona "Permitir Flujo" para restablecer el equilibrio.
- Prueba añadir un producto y observa cómo el exceso presiona el equilibrio hacia los reactivos (Q > Keq).
- Casos especiales: Cambia la simulación al modo "Heterogéneo (S, L, G)". Añade el Sólido (A) o el Líquido (C). Notarás que el nivel de energía no se mueve. Esto ocurre porque los sólidos y líquidos puros tienen una concentración constante (actividad = 1) y no se incluyen en la expresión de Q ni de Keq.
2. Efecto de los cambios en la Presión y Volumen
Teoría: Un aumento de presión (causado por una disminución de volumen) empujará el equilibrio hacia el lado de la ecuación que tenga menor número de moles de gas, minimizando así el aumento de presión. Por el contrario, un aumento de volumen favorecerá la formación de más moles de gas.
Compruébalo en el simulador:
- Haz clic en "Disminuir Volumen". Se abrirá el Análisis Físico Previo, donde verás representados a los reactivos y productos como dos globos bajo un émbolo.
- Observa cómo al apachar el émbolo (aumentar la presión), el globo que revienta primero es el que tiene más gas. Esto es equivalente a que adquiere tanta energía libre que explota.
- Para minimizar esta inestabilidad energética, el sistema responde desplazando el equilibrio en sentido de menos moles. En la reacción de N₂O₄ ⇌ 2NO₂, la compresión favorece la formación del reactivo N₂O₄ (1 mol de gas en los reactivos frente a 2 moles en los productos).
3. Efecto de los cambios en la Temperatura
Teoría: A diferencia de la concentración y la presión, la temperatura es el único factor que altera el valor real de la constante de equilibrio (Keq). Para predecir el desplazamiento, podemos considerar el calor de forma práctica como un reactivo (reacción endotérmica) o como un producto (reacción exotérmica).
Compruébalo en el simulador:
- Selecciona una reacción Exotérmica (libera calor) y haz clic en "Calentar". Observa detenidamente el panel de Desarrollo Termodinámico: el valor de Keq disminuye repentinamente. Como Q ahora resulta ser mayor que la nueva Keq, el sistema se desplaza hacia los reactivos.
- Cambia a una reacción Endotérmica (absorbe calor) y vuelve a calentar. Ahora, el calor extra favorece el proceso directo. Observa cómo Keq aumenta, haciendo que Q < Keq y desplazando el equilibrio hacia los productos.
La clave del principio de Le Chatelier está en la ecuación fundamental de la termodinámica para el equilibrio:
ΔG = RT · ln(Q / Keq)El simulador calcula esta ecuación en tiempo real para cada perturbación que apliques, mostrándote cómo el sistema fluye para que Q iguale a Keq (logaritmo de 1 = 0) y ΔG vuelva a ser cero. ¡Experimenta con diferentes combinaciones hasta dominar el concepto!
Verificación con el Simulador de Partículas (N₂O₄ ⇌ 2NO₂)
Además del tubo en U, puedes comprobar el Principio de Le Chatelier a nivel microscópico utilizando nuestro Simulador Interactivo de Partículas. Ábrelo haciendo clic en el botón flotante naranja (abajo a la derecha) o en el banner, y realiza las siguientes pruebas:
1. Concentración
Prueba: Haz clic en el botón Iniciar y luego aumenta repentinamente los
moles de NO₂ (producto, rojo) usando el control deslizante.
Observación: Al añadir producto repentinamente, el cociente de reacción (Q) se
vuelve mayor que la constante (Keq). En la gráfica inferior notarás que la
línea morada (Q) se dispara por encima de la línea punteada gris (Keq), lo
que indica una inestabilidad por exceso de producto. Para restablecer el equilibrio, el
sistema consumirá el NO₂ extra para formar más N₂O₄ (reactivo, azul) hasta que Q vuelva
a igualar a Keq, demostrando el desplazamiento hacia la izquierda.
2. Presión / Volumen
Prueba: Disminuye drásticamente el Volumen (V) de 750 L a 200 L. Esto aumenta la
presión del sistema.
Observación: Al reducir el espacio, notarás que la línea morada (Q) se dispara
bruscamente hacia arriba. Esto ocurre porque el volumen afecta más a los productos al
estar elevados al cuadrado en la fórmula de Q. Al ser ahora Q > Keq, el
sistema se desplazará hacia donde haya menos moles de gas para aliviar la
presión. Verás la línea morada descender gradualmente mientras se consume el NO₂ rojo a
favor del N₂O₄ azul, hasta que Q regrese a la línea punteada.
3. Temperatura
Prueba: Aumenta la Temperatura (T) de 300 K a 500 K. La disociación del N₂O₄ es
un proceso endotérmico (absorbe calor).
Observación: Al aportar calor, el sistema favorece la reacción directa.
Observarás cómo la línea punteada de Keq sube automáticamente y el gas dentro
del recipiente se vuelve predominantemente rojo (mayor formación de NO₂).
Prueba de Comprensión: Laboratorio Virtual Avanzado
Para consolidar tus conocimientos, interactúa con el Laboratorio Virtual: Variables de Equilibrio (accesible mediante el botón flotante azul o el banner superior). Este simulador servirá de prueba de comprensión del principio de Le Châtelier, desafiándote a predecir y observar los desplazamientos del equilibrio al alterar interactivamente variables como presión, volumen, temperatura y pH en distintos sistemas químicos.
Aplicaciones médicas del Principio de Le Chatelier
- Oxigenoterapia en pacientes con hipoxia: El transporte
de oxígeno en la sangre depende del equilibrio entre la oxihemoglobina y la hemoglobina libre:
Hb + O₂ ⇌ HbO₂. Al aumentar la concentración de O₂ (por ejemplo, administrando oxígeno suplementario), el equilibrio se desplaza hacia la formación de más oxihemoglobina, mejorando la oxigenación de los tejidos. - Intoxicación por monóxido de carbono (CO): El CO compite con el O₂ por la hemoglobina: HbO₂ + CO ⇌ HbCO + O₂. Administrar oxígeno puro o terapia hiperbárica aumenta la concentración de O₂, desplazando el equilibrio y favoreciendo la liberación de CO de la hemoglobina, acelerando la recuperación.
- Equilibrio ácido-base y respiración: El equilibrio CO₂ + H₂O ⇌ H₂CO₃ ⇌ H⁺ + HCO₃⁻ es fundamental en la regulación del pH sanguíneo. Al hiperventilar, disminuye el CO₂, desplazando el equilibrio y reduciendo la concentración de H⁺ (alcalosis). Al hipoventilar, aumenta el CO₂, desplazando el equilibrio hacia la formación de más H⁺ (acidosis).
- Diálisis y eliminación de toxinas: En la diálisis, al reducir la concentración de una sustancia tóxica en la sangre mediante un gradiente de concentración, el equilibrio se desplaza para eliminar más toxina del organismo, siguiendo el principio de Le Chatelier.

Podcast: Definición de Equilibrio Químico
Escucha la explicación sobre la definición de equilibrio químico y su importancia en los sistemas dinámicos.
Video Explicativo: Velocidad de Reacción
Presentación: Velocidad de Reacción
Para mejor experiencia en celular, abre la presentación directamente:
Abrir Presentación PDFVisualiza la presentación de velocidad de reacción.
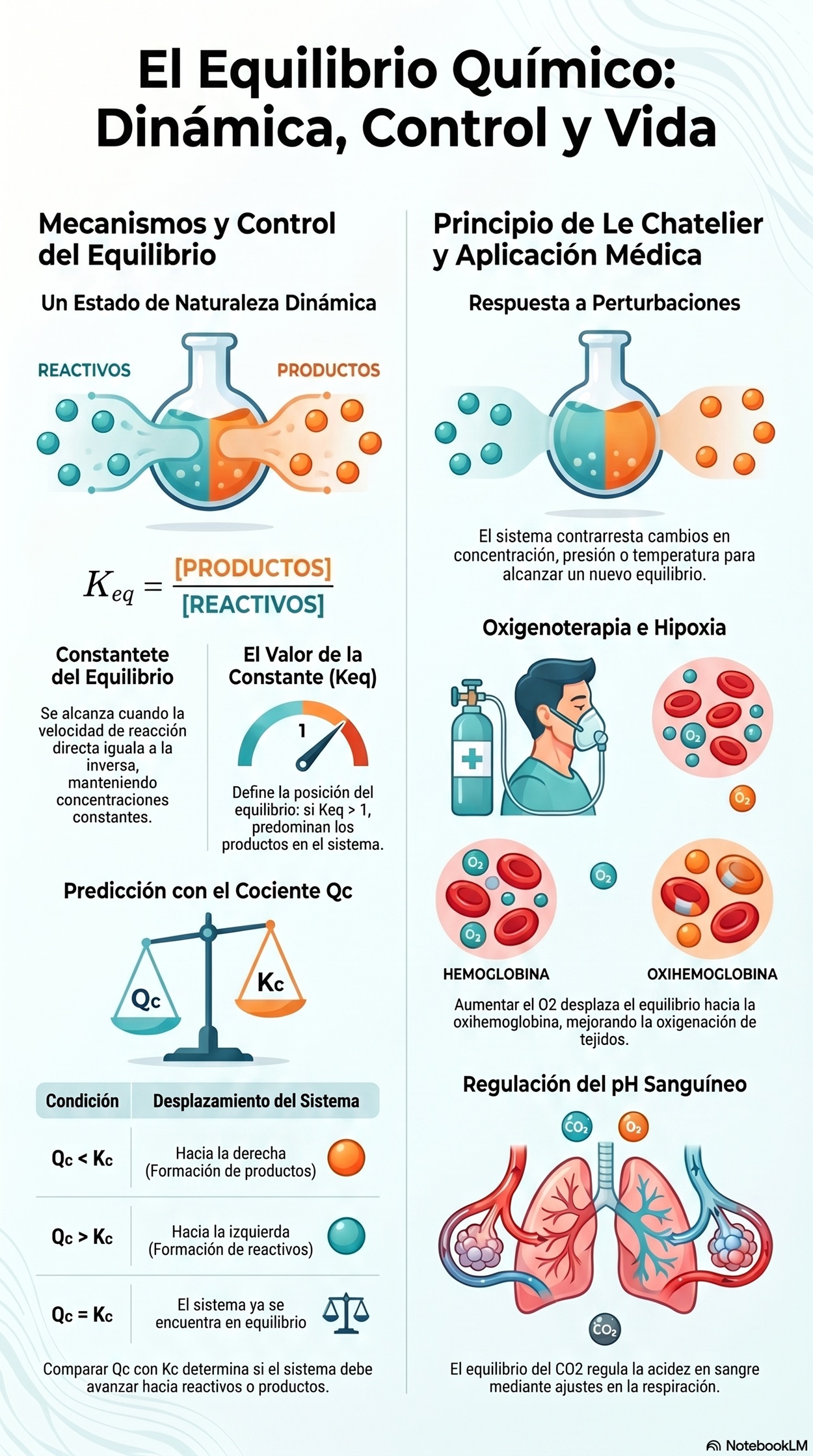
Infografía: Definición de Equilibrio Químico
Resume de forma visual los conceptos clave sobre la definición de equilibrio químico y su importancia.
- 1. ¿Cuándo se dice que un sistema alcanza el equilibrio químico dinámico?
-
Cuando la velocidad de la reacción directa se iguala a la velocidad de la reacción inversa, provocando que las concentraciones de reactivos y productos se mantengan constantes en el tiempo a nivel macroscópico.
- 2. ¿Qué diferencia hay entre la constante de equilibrio (Keq) y el cociente de reacción (Q)?
-
Keq se calcula utilizando únicamente las concentraciones de las sustancias cuando el sistema ya está en equilibrio. Qc se calcula con la misma fórmula, pero usando las concentraciones en cualquier instante (esté o no en equilibrio).
- 3. Si en un instante dado Q < Keq, ¿qué sucederá en el sistema?
-
El sistema no está en equilibrio y le faltan productos. La reacción se desplazará espontáneamente hacia la derecha (hacia los productos) hasta que Q iguale a Keq.
- 4. ¿Cuál es la relación del Principio de Le Châtelier con la energía libre de Gibbs (ΔG)?
-
En equilibrio, ΔG = 0. Al aplicar una perturbación, Q deja de ser igual a Keq, por lo que ΔG ya no es cero. El sistema se desplazará "cuesta abajo" (buscando minimizar la energía libre) hasta restablecer el equilibrio y volver a ΔG = 0.
- 5. ¿Se incluyen las concentraciones de los sólidos y líquidos puros en la expresión de Keq?
-
No. La concentración (o actividad) de los sólidos y líquidos puros se considera constante y ya está incorporada dentro del valor de la propia constante de equilibrio.
- 6. Si calculamos que en un momento dado ΔG > 0 (positivo), ¿hacia dónde se está desplazando la reacción?
-
Un ΔG positivo indica que la reacción directa no es espontánea. El sistema se estará desplazando espontáneamente hacia la izquierda (hacia los reactivos) para alcanzar el equilibrio.
- 7. ¿Un catalizador puede cambiar el valor de Keq o la posición del equilibrio final?
-
No. El catalizador acelera tanto la reacción directa como la inversa en la misma proporción. Solo disminuye el tiempo necesario para alcanzar el equilibrio, pero no altera las cantidades finales ni el valor de Keq.
- 8. Si se añade un producto adicional a un sistema en equilibrio, ¿cómo será el valor de Q respecto a Keq en ese instante?
-
El valor de Q será mayor que Keq (Q > Keq) porque el numerador (productos) de la expresión matemática ha aumentado artificialmente.
-
Explique detalladamente por qué el estado de equilibrio químico se describe como
"dinámico" y no "estático", apoyándose en lo que observó en el simulador de
partículas.
Debe mencionarse que, a nivel macroscópico, las concentraciones ya no cambian (parece estático), pero a nivel microscópico, las moléculas de reactivos siguen chocando para formar productos y viceversa. Se llama "dinámico" porque ambas reacciones continúan ocurriendo simultáneamente y a la misma velocidad. -
Mencione un ejemplo de cómo se aplica el Principio de Le Châtelier en un caso médico
(como la oxigenoterapia o alteraciones del pH).
Al administrar O₂ suplementario en hipoxia, se aumenta la concentración del reactivo en el equilibrio de la hemoglobina, forzando al sistema a desplazarse a la derecha para formar más oxihemoglobina (HbO₂), mejorando así la oxigenación en los tejidos. -
Compare el concepto de equilibrio químico en un sistema cerrado con el estado
estacionario (homeostasis) de un sistema biológico abierto celular.
En el equilibrio químico clásico (sistema cerrado) las concentraciones no cambian y no hay flujo neto de materia/energía (ΔG=0). En el estado estacionario biológico, las concentraciones se mantienen constantes gracias a un aporte continuo de energía y materia desde el exterior, manteniendo al sistema alejado del equilibrio verdadero (ΔG < 0). -
Describa cómo utilizaría la ecuación matemática ΔG = RT ln(Q/Keq) para explicar por
qué la reacción macroscópica se "detiene" justo cuando Q alcanza el valor de Keq.
Cuando las concentraciones cambian hasta que Q se iguala a Keq, la relación Q/Keq se vuelve 1. El logaritmo natural de 1 es cero (ln 1 = 0), lo que resulta en un ΔG = 0. Sin energía libre disponible, el sistema ya no tiene potencial para realizar trabajo ni para cambiar la proporción de productos y reactivos.
-
Escriba la expresión de la constante de equilibrio (Keq) para la siguiente reacción
química balanceada:
aA + bB ⇌ cC + dD
La constante se expresa con los productos en el numerador y los reactivos en el denominador, elevados a sus coeficientes:
Keq = [C]c[D]d / [A]a[B]b -
Para una reacción general, el valor de Keq es 4.5 × 104. ¿Qué se puede
concluir sobre las cantidades de reactivos y productos en el equilibrio?
Como Keq es un número muy grande (mayor a 1), significa que en el estado de equilibrio la concentración de los productos es mucho mayor que la de los reactivos (el equilibrio está fuertemente desplazado hacia la derecha). -
Escriba la expresión de Kc para la reacción de descomposición del tetraóxido de
dinitrógeno: N2O4(g) ⇌ 2NO2(g).
El dióxido de nitrógeno es el producto y tiene coeficiente 2, por lo que su concentración va al cuadrado en el numerador:
Kc = [NO2]2 / [N2O4] -
Para una mezcla de reacción se calcula un Qc = 50, mientras que la constante Keq de
esa reacción a esa temperatura es 10. ¿Se formarán más reactivos o más productos a
medida que el sistema avance hacia el equilibrio?
Como Qc > Keq (50 > 10), la proporción de productos es demasiado alta respecto al equilibrio. Por lo tanto, el sistema se desplazará hacia la izquierda y se formarán más reactivos para reducir el valor de Q hasta que sea 10. -
Plantee la expresión de la constante de equilibrio para la combustión incompleta del
carbono sólido: 2C(s) + O2(g) ⇌ 2CO(g)
El C(s) no se incluye en la fórmula por ser un sólido puro. La expresión es:
Keq = [CO]2 / [O2]