Instrucciones
Usted tiene las siguientes opciones en este simulador para moléculas pequeñas tanto inorgánicas como orgánicas.
- En la parte superior, aparecen los botones 2D y 3D para que pueda observar el modelo en dos o tres dimensiones.
- A continuación se presenta el modelo en dos o tres dimensiones.
- "Search" puede ser utilizado para buscar alguna molécula, escribiendo el nombre en inglés, por ejemplo al escribir, sulphuric acid (ácido sulfúrico).
- Color de fondo, sirve seleccionar el color del fondo del modelo en tres dimensiones.
- Girar X, Y, Z, para girar el modelo en tres dimensiones en los ejes x, y, z.
- Alambres, varillas y pelotas y varillas, para cambiar el modelo en tres dimensiones en esas representaciones.
- Energía, aparce en la parte superior la energía de la molécula en kJ/mol o kcal/mol.
- Minmizar por MMFF94, normalmente las estructuras iniciales que se crean en los simuladores poseen energías mucho mayores a las que tendría un objeto real, por esta razón, se utilizan algoritmos para calcular las posiciones y fuerzas originales, con el objetivo de minimizarlas y que sean más realistas.
- Arrastrar Minimizar, usted puede arrastrar un átomo, soltarlo y entonces el sistema hace un cálculo de minimización de energía.
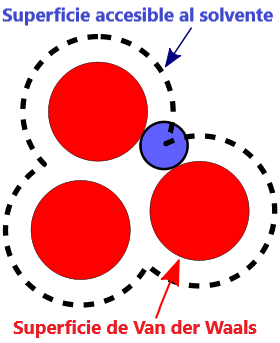
- Superficie VDW, La superficie de van der Waals de una molécula es una representación abstracta o modelo de esa molécula, que ilustra dónde, en términos muy generales, podría haber una superficie para la molécula en función de los cortes duros de los radios de van der Waals para átomos individuales, y representa una superficie a través de la cual la molécula podría concebirse interactuando con otras moléculas.
- PEM es el mapa de potencial electrostático.
- Cargas parciales, para ver el valor de la carga relativa positiva o negativa de cada átomo.
- Tetraedros, para el caso que exista alguna átomo tetraédrico.
- Dipolos enlaces, para ver el los dipolos de todos los enlaces.
- Dipolo molecular, para ver el momento dipolar resultante de toda la molécula.
- Botón 2D, cuando escoge el botón 2D, la aplicación tiene su propio menú y quedan inhabilitados todos los botones 3D.
Laboratorio de IA: Tu Copiloto de Estudio
Usa IA para profundizar en el equilibrio heterogéneo y homogéneo
Estos prompts están diseñados para ayudarte a explorar los conceptos clave de equilibrio químico, especialmente la diferencia entre sistemas homogéneos y heterogéneos, el papel de los sólidos y la interpretación de la constante de equilibrio.
1. Diferencia entre equilibrio homogéneo y heterogéneo
Fases presentes y cómo se plantea la constante de equilibrio.
2. Importancia de los sólidos en el equilibrio heterogéneo
¿Por qué no se incluyen en la expresión de Kc?
3. Ejemplo de cálculo de Kc en equilibrio heterogéneo
Plantea la expresión y resuelve un caso sencillo.
Equilibrio Químico
Conceptos de Química: Equilibrio Heterogéneo
¿Qué es el Equilibrio Heterogéneo?
El equilibrio heterogéneo se presenta en una reacción reversible en la que las sustancias que intervienen (reactivos y productos) se encuentran en más de una fase o estado físico (por ejemplo, interacciones entre sólidos y gases, o líquidos y gases).
Nota importante: En las expresiones de la constante de equilibrio (Kc o Kp) para estos sistemas, no se incluyen las concentraciones de los sólidos puros ni de los líquidos puros, ya que sus concentraciones se mantienen constantes a una temperatura dada.
Ejemplo representativo: Descomposición del Carbonato de Calcio
CaCO3(s) ⇌ CaO(s) + CO2(g)
Más Ejemplos de Equilibrio Heterogéneo
1. Sistema con Tres Estados (Sólido, Líquido y Gas)
Proceso de formación de cavernas (Ej. Semuc Champey / Lanquín)
CaCO3(s) + H2O(l) + CO2(g) ⇌ Ca2+(ac) + 2HCO3-(ac)
Este sistema geológico y químico involucra reactivos en estado sólido (piedra caliza), líquido (agua) y gaseoso (dióxido de carbono del aire o suelo). Es el responsable de la disolución de la roca calcárea.
2. Equilibrio de Solubilidad
Cloruro de Plata en agua
AgCl(s) ⇌ Ag+(ac) + Cl-(ac)
Interacción entre una fase sólida (un precipitado o sal poco soluble) y una fase acuosa (los iones disueltos).
Correlación Clínica: El Equilibrio en el Cuerpo Humano
Para los futuros médicos, comprender el equilibrio heterogéneo es vital para entender diversas patologías y procesos fisiológicos.
Nefrolitiasis (Cálculos Renales)
Precipitación de Oxalato de Calcio en la orina
CaC2O4(s) ⇌ Ca2+(ac) + C2O42-(ac)
Cuando la concentración de iones calcio y oxalato en la orina supera el límite de solubilidad (su Kps), el equilibrio se desplaza hacia la izquierda, formando cristales sólidos que se agrupan para formar las dolorosas "piedras en los riñones".
Fisiología Respiratoria
Intercambio de Oxígeno en los alvéolos
O2(g) ⇌ O2(ac)
En los pulmones, existe un equilibrio vital entre el oxígeno en estado gaseoso dentro de los alvéolos y el oxígeno disuelto en fase acuosa en el plasma sanguíneo, antes de unirse a la hemoglobina. Este equilibrio obedece a la Ley de Henry.
Mineralización Ósea
Hidroxiapatita en hueso
Ca10(PO4)6(OH)2(s) ⇌ 10Ca2+ + 6PO43- + 2OH-
Kps = [Ca2+]10[PO43-]6[OH-]2
La hidroxiapatita es el principal mineral del hueso. Su equilibrio de solubilidad explica la osteoporosis: cuando el aporte de Ca2+ disminuye, el equilibrio se desplaza a la derecha disolviendo el hueso.
Tampón CO2 / Bicarbonato
Sistema tampón principal de la sangre
CO2(g) ⇌ CO2(aq) ⇌ H2CO3(ac) ⇌ H+(ac) + HCO3-(ac)
pH = pKa + log([HCO3-] / [CO2])
Este equilibrio de fases (gas ⇌ acuoso) regula el pH de la sangre (7.35–7.45). Alteraciones producen acidosis (pH < 7.35) o alcalosis (pH > 7.45), con consecuencias clínicas graves.
Colelitiasis (Cálculos Biliares)
Saturación de colesterol en bilis
Colesterol(s) ⇌ Colesterol(aq)
Kps = [Colesterol(aq)]
Cuando la bilis se sobresatura de colesterol (Q > Kps), éste precipita formando cálculos sólidos. Es el tipo más frecuente de cálculo biliar y causa la mayoría de las colecistitis agudas.
Concepto Clave para el Clínico: Q vs Kps
El producto de solubilidad (Kps) determina si una sal precipita en los fluidos corporales. Cuando el producto iónico (Q) supera el Kps, el sistema se desplaza hacia la izquierda y se produce precipitación — este es el mecanismo detrás de los cálculos renales, cálculos biliares y la calcificación patológica de tejidos blandos (calcifilaxis).
Resumen Comparativo: Equilibrio Homogéneo vs. Heterogéneo
| Característica | Equilibrio Homogéneo | Equilibrio Heterogéneo |
|---|---|---|
| Fases presentes | Una sola fase | Dos o más fases |
| Ejemplo típico | N2(g) + 3H2(g) ⇌ 2NH3(g) | CaCO3(s) ⇌ CaO(s) + CO2(g) |
| Expresión de K | Incluye todas las especies | Excluye sólidos y líquidos puros |
| ¿Por qué se excluyen sólidos/líquidos? | — | Su concentración es constante a T y P fijas; se absorbe dentro del valor de K |
| Ejemplo clínico | Hemoglobina: Hb + O2(aq) ⇌ HbO2 | Nefrolitiasis: CaC2O4(s) ⇌ Ca2+(ac) + C2O42-(ac) |
Tipos de Equilibrio y sus Expresiones de K
| Tipo | Reacción | Expresión de K | Notas |
|---|---|---|---|
| Homogéneo gaseoso | N2(g) + 3H2(g) ⇌ 2NH3(g) | K = [NH3]2 / ([N2][H2]3) | Todas las especies en fase gas |
| Heterogéneo (sólido-gas) | CaCO3(s) ⇌ CaO(s) + CO2(g) | K = [CO2] | CaCO3 y CaO excluidos |
| Heterogéneo (gas-líquido) | NH3(g) + H2O(l) ⇌ NH4+(ac) + OH-(ac) | K = [NH4+][OH-] / [NH3] | H2O líquida excluida |
| Solubilidad (Kps) | AgCl(s) ⇌ Ag+(ac) + Cl-(ac) | Kps = [Ag+][Cl-] | AgCl sólido excluido |
Equilibrio Químico Heterogéneo
Comprendiendo la termodinámica y cinética en sistemas con múltiples fases
1. Acceso al Laboratorio Virtual
Para explorar la dinámica de esta reacción interactiva, note que en la parte superior de esta página se encuentra el enlace directo al laboratorio virtual de equilibrio heterogéneo.
2. ¿Por qué utilizar este simulador?
En la enseñanza de la química (especialmente en áreas aplicadas como las ciencias de la salud y la formación docente), es un desafío lograr que los estudiantes visualicen por qué un exceso de reactivo sólido no desplaza el equilibrio.
- Ruptura de preconceptos: Los estudiantes suelen aplicar el Principio de Le Chatelier a ciegas, creyendo que agregar más \(CaCO_3\) desplazará la reacción hacia la derecha. El simulador les demuestra gráficamente que esto es falso.
- Conexión macro-micro: Permite ver el reactor (los montículos de rocas y polvo) y simultáneamente observar la gráfica matemática de la concentración del gas en tiempo real.
- Dinámica de sistemas: Ayuda a comprender que el equilibrio no es estático; si extraemos \(CO_2\), el sistema reacciona cinéticamente consumiendo \(CaCO_3\) para restaurar el valor de \(K_c\).
3. Guía de Uso del Simulador
Siga estos pasos para explorar la dinámica del equilibrio con sus estudiantes:
- Observe el estado inicial: Note cómo la gráfica muestra que la concentración de \([CO_2]\) busca estabilizarse en la línea punteada negra que representa el valor de \(K_c\).
-
Perturbe los sólidos (La trampa pedagógica):
Haga clic en "+ Agregar" en el \(CaCO_3\) o el \(CaO\).
¿Qué observa? El montículo en el reactor crece visiblemente, pero la gráfica de \(CO_2\) ni se inmuta. Esto confirma empíricamente la exclusión de los sólidos en la expresión de \(K_c\). -
Perturbe el gas (Le Chatelier en acción):
Haga clic en "- Extraer" en el \(CO_2\).
Al disminuir \([CO_2]\), el sistema pierde el equilibrio (\(Q_c < K_c\)). Note cómo el simulador automáticamente empieza a consumir el montículo rocoso de \(CaCO_3\) para producir más gas hasta alcanzar \(K_c\) nuevamente. -
Reactivo Limitante:
Extraiga continuamente \(CO_2\) hasta que el montículo de \(CaCO_3\) desaparezca por
completo.
Si no hay sólido reactante, el equilibrio se rompe y el sistema no puede restaurar la concentración del gas.

Podcast: Definición de Equilibrio Químico
Escucha la explicación sobre la definición de equilibrio químico y su importancia en los sistemas dinámicos.
Video Explicativo: Equilibrio Químico Heterogéneo
Presentación: Equilibrio Químico Heterogéneo
Para mejor experiencia en celular, abre la presentación directamente:
Abrir Presentación PDFVisualiza la presentación de equilibrio químico heterogéneo.
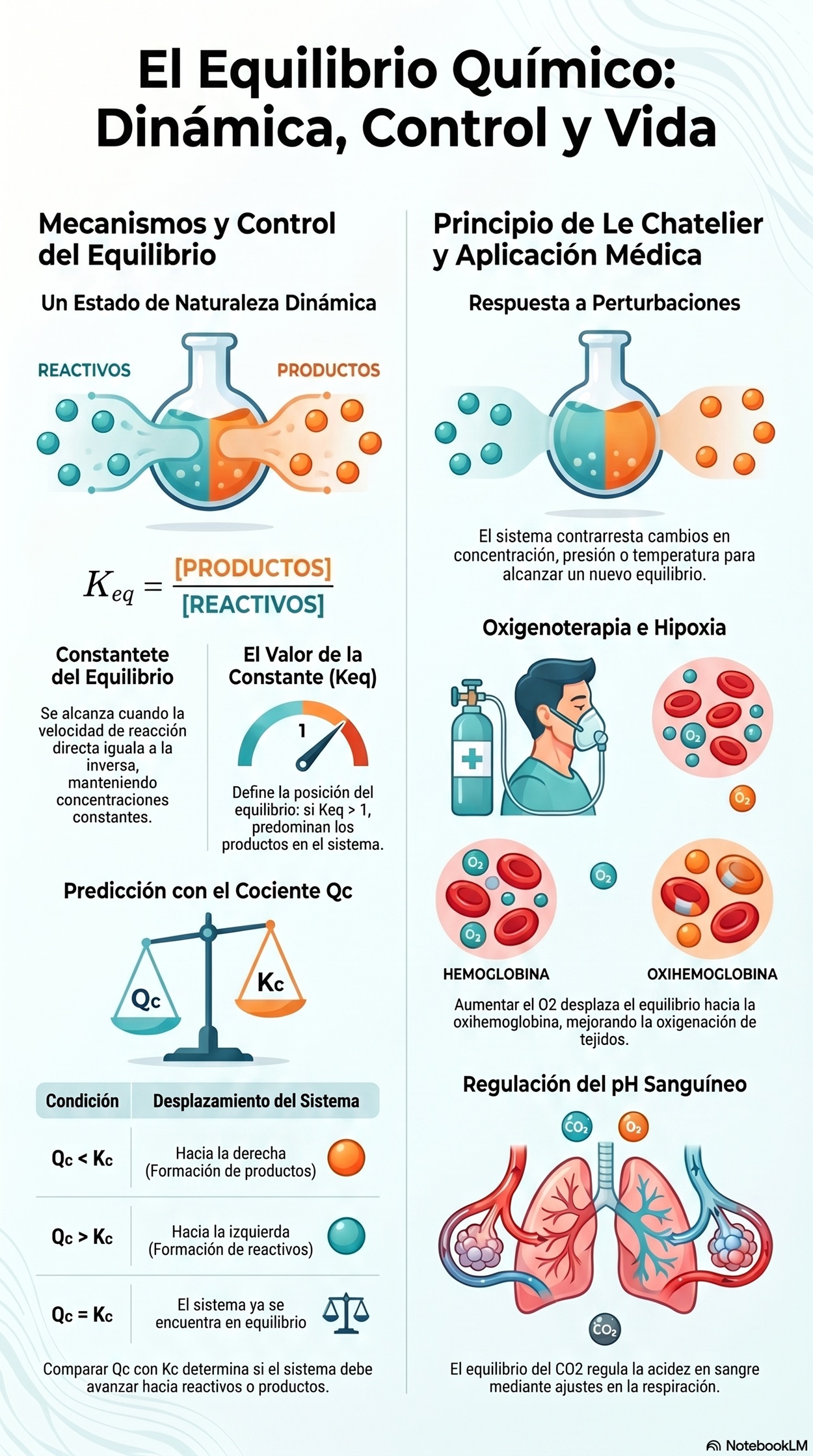
Infografía: Equilibrio Químico Heterogéneo
Resume de forma visual los conceptos clave sobre el equilibrio heterogéneo y su importancia en los sistemas con múltiples fases.
- 1. ¿Cuál es la diferencia fundamental entre un equilibrio homogéneo y uno heterogéneo?
- 2. ¿Por qué no se incluyen los sólidos y líquidos puros en la expresión de la constante de equilibrio (Kc o Kps) de un sistema heterogéneo?
- 3. Plantee la expresión de Kc para la reacción CaCO₃(s) ⇌ CaO(s) + CO₂(g). ¿Qué especies aparecen y por qué?
- 4. ¿Qué ocurre si se agrega más sólido (por ejemplo, CaCO₃) a un sistema en equilibrio heterogéneo?
- 5. ¿Cómo se relaciona el producto iónico Q y el Kps en la formación de precipitados (como cálculos renales o biliares)?
-
Analiza la importancia clínica del equilibrio heterogéneo usando el ejemplo de cálculos
renales o biliares. ¿Cómo ayuda el concepto de Kps y Q a entender la formación de estos
precipitados en el cuerpo?
-
Explica cómo el equilibrio heterogéneo está presente en la fisiología respiratoria
(intercambio de gases en los pulmones) o en el sistema tampón CO₂/bicarbonato de la
sangre.
-
Mencione dos ejemplos de equilibrio heterogéneo relevantes en medicina y explique cómo
el concepto de Kps se aplica en cada uno.
-
Compare el equilibrio homogéneo con el heterogéneo en términos de cómo se construye la
expresión de Keq.
-
Escriba la expresión de Keq para: aA + bB ⇌ cC + dD
-
Escriba la expresión de Keq para: Fe(OH)3(s) ⇌ Fe3+(ac) +
3OH−(ac)
-
Escriba la expresión de Kc para: 2SO2(g) + O2(g) ⇌
2SO3(g)
-
Escriba la expresión de Kc para: Ca3(PO4)2(s) ⇌
3Ca2+(ac) + 2PO43−(ac)
-
Plantee la expresión de Keq para: 2C(s) + O2(g) ⇌ 2CO(g)